Acetylocholina
| Formuła strukturalna | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
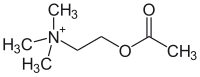
| |||||||||||||
| Nie pokazano przeciwjonu (głównie chlorku) | |||||||||||||
| Generał | |||||||||||||
| Nazwa niezastrzeżona | Acetylocholina | ||||||||||||
| inne nazwy |
|
||||||||||||
| Formuła molekularna | C 7 H 16 NO 2 | ||||||||||||
| Krótki opis |
biały, krystaliczny proszek lub bezbarwne kryształki, bardzo higroskopijny (chlorek) |
||||||||||||
| Identyfikatory zewnętrzne / bazy danych | |||||||||||||
| |||||||||||||
| Informacje o narkotykach | |||||||||||||
| Kod ATC | |||||||||||||
| Klasa leków | |||||||||||||
| nieruchomości | |||||||||||||
| Masa cząsteczkowa | |||||||||||||
| Stan fizyczny |
mocno |
||||||||||||
| Temperatura topnienia |
149-152 ° C (chlorek) |
||||||||||||
| rozpuszczalność |
bardzo łatwo rozpuszczalny w wodzie, słabo rozpuszczalny w etanolu , słabo rozpuszczalny w dichlorometanie (chlorku) |
||||||||||||
| instrukcje bezpieczeństwa | |||||||||||||
| |||||||||||||
| Dane toksykologiczne | |||||||||||||
| W miarę możliwości i zwyczajowo stosowane są jednostki SI . O ile nie zaznaczono inaczej, podane dane dotyczą warunków standardowych . | |||||||||||||
Acetylocholina ( ACh ) jest jednym z najważniejszych neuroprzekaźników wielu organizmów, w tym człowieka . Czwartorzędowy związek amoniowy acetylocholiny jest ester z kwasem octowym i jednowodorotlenowego alkoholu amino choliny .
historia
W 1921 roku Otto Loewi zademonstrował za pomocą żabiego serca, że za przekazywanie impulsu nerwowego do serca odpowiada substancja chemiczna, którą początkowo nazwał substancją błędną, a którą Henry H. Dale zidentyfikował później jako acetylocholinę.
Substancja została po raz pierwszy zsyntetyzowana w 1867 roku przez Adolfa Baeyera , za pomocą którego amerykański Reid Hunt (1870-1948) był w stanie wywołać skurcze mięśni w doświadczeniach na zwierzętach.
Występowanie
Acetylocholina znajduje się zarówno w ośrodkowym, jak i obwodowym układzie nerwowym .
W autonomicznym układzie nerwowym jest przekaźnikiem wszystkich neuronów przedzwojowo-autonomicznych. Pośredniczy również w przekazywaniu sygnałów z postganglionowych neuronów przywspółczulnych do narządów końcowych. Zazwojowe neurony współczulne normalnie wykorzystują noradrenalinę , wyjątek stanowią drogi prowadzące do gruczołów potowych, które również wykorzystują ACh jako przekaźnik.
W obwodowym układzie nerwowym ACh pośredniczy w przenoszeniu pobudzenia z nerwów do mięśni poprzez płytkę nerwowo-mięśniową .
W ośrodkowym układzie nerwowym ACh znajduje się w ciele prążkowanym , w jądrze podstawnym Meynerta z kanałami do kory mózgowej oraz w przegrodzie formowanej z kanałami do hipokampa . Po kwasie γ-aminomasłowym (GABA) i glicynie, acetylocholina jest jednym z najczęstszych neuroprzekaźników w mózgu .
funkcjonować
Funkcja komórkowa
Acetylocholiny działa na dwóch rodzajach cholinergicznymi receptorami , na nikotynowy receptor acetylocholiny i receptory muskarynowe . Swoją nazwę wzięły od substancji, które specyficznie je aktywują, nikotyna dla receptora nikotynowego i muskarynowa dla receptora muskarynowego. Istnieją różne podtypy obu.
Receptor nikotynowy ACh jest kontrolowanym przez ligand kanał jonowy, który po otwarciu, tj. po związaniu ACh, jest przepuszczalny dla jonów sodu, potasu i wapnia. Istnieją dwa podtypy receptora, typ mięśniowy, który może być selektywnie hamowany przez kurarę i typ neuronowy, który może być selektywnie hamowany przez heksametonium .
Receptor muskarynowy ACh jest receptorem sprzężonym z białkiem G z 5 podtypami (M1-M5). M1, M3 i M5 są G Q -coupled, M2 i M4 G I / G O -coupled.
Istnieją również substancje, które mogą pośrednio nasilać działanie ACh na jego receptory (pośrednio substancje cholinergiczne). Należą do nich różne inhibitory cholinesterazy (właściwie inhibitory acetylocholinesterazy). To bardzo różne substancje hamujące. Wymienione wyżej leki stosowane w chorobie Alzheimera należą do dużej grupy tych substancji. Niektóre powodują tymczasowe zahamowanie, inne trwale blokują enzym. Takimi nieodwracalnie działającymi inhibitorami cholinoesterazy są różne estry kwasu fosforoorganicznego , m.in. B. znany insektycyd Parathion (E 605), ale także chemiczne środki bojowe sarin , tabun , Novitschok i wiele innych, które w niewielkich ilościach powodują śmiertelną nadmierną stymulację synaps cholinergicznych. Substancja neostygmina należy do grupy odwracalnych inhibitorów cholinesterazy . Wiele substancji blokuje również działanie acetylocholiny na jej receptory (zwłaszcza na receptory muskarynowe); nazywa się to wtedy efektem antycholinergicznym . Pewne alkaloidy mają działanie antycholinergiczne, na przykład, atropiny lub hioscyaminę lub skopolamina .
Inhibitory cholinesterazy, takie jak paration czy neostygmina, są również stosowane jako antidotum na kurarę . Kurare blokuje punkty dokowania acetylocholiny na płytkach motorycznych i tym samym paraliżuje mięśnie szkieletowe, co prowadzi do śmierci przez uduszenie. Ponieważ aktywne składniki Curare są konkurencyjnymi blokerami, dużo acetylocholiny może je wypierać. Jeśli acetylocholinesteraza jest teraz zablokowana, więcej acetylocholiny pozostaje w szczelinie synaptycznej i transmisja działa ponownie. Ponieważ stężenie acetylocholiny wzrasta również na receptorach muskarynowych, często konieczne jest dalsze leczenie atropiną. Efekt ten stosuje się również w znieczuleniu ogólnym : przed operacją mięśnie są sparaliżowane blokerem nerwowo-mięśniowym (np. rokuronium ). Odwracalny inhibitor cholinesterazy (np. neostygmina) jest podawany w celu odwrócenia jego działania. Ponadto do odwrócenia muskarynowych skutków ubocznych stosuje się parasympatykolityczny (np. atropinę).
Fizostygmina (eseryna) jest również inhibitorem cholinoesterazy i zapobiega rozkładowi acetylocholiny przez cholinoesterazę na cholinę i octan.
Funkcja w ośrodkowym układzie nerwowym
W ośrodkowym układzie nerwowym ACh odgrywa ważną rolę w zwiększaniu czuwania, utrzymywaniu czujności, uczeniu się i tworzeniu wspomnień.
Biosynteza i metabolizm
Acetylocholina jest tworzona z acetylo-CoA i choliny przez enzym acetylotransferazę cholinową .
Gotowy ACh jest pobierany z cytozolu do neurosekrecyjnych pęcherzyków magazynujących poprzez antyporter protonowy/acetylocholinowy w błonie pęcherzyka . Każdy pęcherzyk zawiera od 5000 do 10 000 cząsteczek acetylocholiny. W jednej synapsie znajduje się około miliona pęcherzyków magazynujących.
Enzym acetylocholinoesteraza , po uwolnieniu do szczeliny synaptycznej i związaniu z receptorem acetylocholiny , może zostać ponownie rozdzielony na cholinę i kwas octowy (lub octan ) i unieszkodliwiony.
Zapewnienie początkowych cząsteczek do tworzenia acetylocholiny
Cholina może być ponownie pobierana do synapsy z luki synaptycznej za pośrednictwem symportera sodowo-choliny i jest produktem rozpadu acetylocholiny uwolnionej jako ostatni. Dostępność i wychwyt choliny stanowi etap ograniczający szybkość syntezy ACh, ponieważ nie może być ona wytwarzana przez samą komórkę nerwową.
Pirogronian jest końcowym produktem glikolizy w cytozolu każdej komórki. Enzym dehydrogenaza pirogronianowa katalizuje konwersję pirogronianu do acetylokoenzymu A. Ponieważ acetylo-CoA nie może zajść wewnętrzna błona mitochondrialna , jest on zasilany w cyklu kwasu cytrynowego i poprzez reakcję ze szczawiooctanem (katalizowanym przez syntazę cytrynianową ) w cytrynian przekształcany. Cytrynian przechodzi przez błonę mitochondrialną i jest ponownie rozkładany na acetylo-CoA i szczawiooctan przez liazę cytrynianową . Acetylo-CoA jest zatem dostępny do tworzenia acetylocholiny.
Choroby związane z układem cholinergicznym
W chorobie Alzheimera śmierć komórek nerwowych wytwarzających głównie acetylocholinę powoduje niedobór acetylocholiny. Próbuje się wyrównać ten niedobór lekami, stosując inhibitory acetylocholinesterazy hamujące ten enzym rozkładający acetylocholinę w celu zwiększenia stężenia acetylocholiny w synapsach . Innym sposobem jest podawanie takich białek prekursorowych . B. Deanol i Meclophenoxat , aby podnieść poziom świadomości.
Zwiększona akumulacja acetylocholiny w wyniku zmniejszonego rozkładu substancji powoduje kryzys cholinergiczny .
W myasthenia gravis osłabienie mięśni , poważna choroba autoimmunologiczna, wytwarzane są przeciwciała, które niszczą receptory acetylocholiny w komórkach mięśniowych, a tym samym osłabiają aktywność mięśni. Może to posunąć się do tego stopnia, że pacjenci nie będą mogli dłużej mieć otwartych oczu.
Acetylocholina w truciznach zwierzęcych i roślinnych
Udział acetylocholiny w truciźnie szerszeni ( Vespa crabro ) wynosi około 6% suchej masy, a zatem jest to najwyższe stężenie, jakie stwierdzono u żywej istoty. Ukąszenie szerszenia jest odbierane jako szczególnie bolesne ze względu na wysoką koncentrację. Żądło nie jest bardziej trujące niż innych os czy pszczół ( jad pszczeli ), których jad nie zawiera acetylocholiny. Acetylocholina jest również odpowiedzialna za bolesne działanie w truciznach pokrzyw , skrzydlic i innych skorpionów .
posługiwać się
W okulistyce acetylocholina stosowana jest w celu zwężenia i zmiany położenia powiększonej przedoperacyjnie źrenicy po usunięciu soczewki podczas operacji zaćmy , irydektomii , perforacji keratoplastyki i innych zabiegów na przednim odcinku oka, jeśli wymaga to bardzo szybkiego i całkowitego zwężenia źrenicy .
Zgodnie z Dyrektywą Kosmetyczną WE, acetylocholina nie może być składnikiem produktów kosmetycznych .
Zobacz też
Indywidualne dowody
- ↑ a b c Karta katalogowa Acetylcholine Chloride CRS (PDF) w EDQM , dostęp 24 stycznia 2009 r.
- ↑ Karta charakterystyki acetylocholiny firmy Acros, dostęp 22 lutego 2010 r.
- ↑ a b Karta danych Chlorek acetylocholiny firmy Sigma-Aldrich , dostęp 2 marca 2019 r. ( PDF ).
- ↑ Otto Westphal , Theodor Wieland , Heinrich Huebschmann: regulator życia. Hormony, witaminy, fermenty i inne aktywne składniki. Societäts-Verlag, Frankfurt am Main 1941 (= Frankfurter Bücher. Research and Life. Tom 1), s. 33 i 81 f.
- ↑ Barbara E. Jones: Od jawy do snu: substraty neuronalne i chemiczne . W: Trendy w naukach farmakologicznych . taśma 26 , nie. 11 , listopad 2005, s. 578-586 , doi : 10.1016 / j.tips.2005.09.09 , PMID 16183137 .
- ↑ AM Himmelhub, M. Sarter, JP Bruno: Zwiększenie uwalniania acetylocholiny w korze podczas długotrwałego działania uwagi u szczurów . W: Badania mózgu. Badania poznawcze mózgu . taśma 9 , nie. 3 , 2000, s. 313-325 , PMID 10808142 .
- ↑ RM Ridley, PM Bowes, HF Baker, TJ Crow: Zaangażowanie acetylocholiny w uczeniu się rozróżniania obiektów i pamięci u marmozet . W: Neuropsychologia . taśma 22 , nie. 3 , 1984, s. 253-263 , PMID 6431311 .
- ^ PT Francis, AM Palmer, M. Snape, GK Wilcock: Hipoteza cholinergiczna choroby Alzheimera: przegląd postępu . W: Journal of Neurology, Neurosurgery and Psychiatry . taśma 66 , nie. 2 , 1999, s. 137-147 , PMID 10071091 , PMC 1736202 (wolny pełny tekst).
- ↑ Eric Kandel: W poszukiwaniu pamięci, 2009 3. wydanie, Goldmann, Monachium

