Aminotransferazy
| Aminotransferazy | ||
|---|---|---|

| ||
| Model wstążkowy transaminazy asparaginianowej według PDB 1AAM | ||
| Klasyfikacja enzymów | ||
| WE, kategoria | 2.6.1.- , transferazy | |
| Typ odpowiedzi | Transfer grup aminowych ( transaminacja ) | |
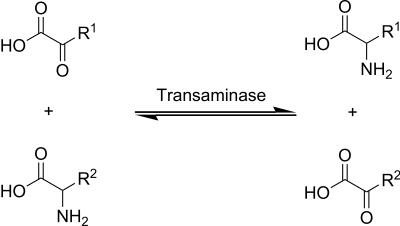
Aminotransferazy lub transaminazy to enzymy występujące we wszystkich żywych organizmach, które katalizują przeniesienie grup α- aminowych z cząsteczki dawcy do cząsteczki akceptora ( transaminacja ).
cechy
W medycznego badania laboratoryjne na transaminaz jest pomiar stężenia we krwi dla aminotransferazy asparaginianowej (ASAT) i aminotransferazy alaninowej (ALAT) , znaczenie diagnostyczne w chorobach wątroby mają ( transaminazę ) .
Transaminazy są niezbędne w metabolizmie aminokwasów i biosyntezie heksozaminy . Ponadto aminotransferaza glutaminian-1-semialdehydu bierze udział w biosyntezie porfiryn u bakterii i archeonów . Transaminazy są hamowane przez inhibitory transaminaz .
Katalizowana reakcja
Dawcą jest zazwyczaj aminokwas, a akceptorem jest α- ketokwas , aminokwas staje się nowym α-ketokwasem, a oryginalny α-ketokwas nowym aminokwasem. W wielu przypadkach fosforan pirydoksalu jest zaangażowany jako kofaktor .
Transaminazy są dostępne dla 19 z 20 aminokwasów proteinogennych, co oznacza, że są one w rzeczywistości tylko częściowo niezbędne. Można je przekształcić ze specjalnych ketokwasów, z których część jednak nie jest dostarczana przez metabolizm. Aminokwasem partnerskim jest zwykle glutaminian , który jest deaminowany do α- ketoglutaranu i tym samym służy jako uniwersalny donor grup aminowych. Dlatego glutaminian jest zwykle pomijany w nazewnictwie transaminazy.
literatura
- Ulf Dettmer, Malte Folkerts, Eva Kächler, Andreas Sönnichsen: Intensywny kurs biochemii (Elsevier-Verlag, Monachium, 1. wydanie 2005, ISBN 978-3437444500 )
- Smith DM, Thomas NR, Gani D: Porównanie enzymów dekarboksylazy zależnej od pirydoksalu 5'-fosforanu i transaminazy na poziomie molekularnym . W: Experientia . 47, nr 11-12, grudzień 1991, str. 1104-18. PMID 1765122 .
- Rossi F, Schwarcz R, Rizzi M: Curiosity to kill the KAT (kynurenine aminotransferase): strukturalny wgląd w syntezę kwasu kinureninowego mózgu . W: Curr. Opin. Struct. Biol . 18, nr 6, grudzień 2008, s. 748-55. doi : 10.1016 / j.sbi.2008.09.009 . PMID 18950711 .
- Yonaha K, Nishie M, Aibara S: Podstawowa struktura aminokwasu omega: aminotransferaza pirogronianowa . W: J. Biol, Chem . 267, nr 18, czerwiec 1992, str. 12506-10. PMID 1618757 .