Azirine
| Formuła strukturalna | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||
| Generał | |||||||||||||
| Nazwisko | Azirine | ||||||||||||
| inne nazwy |
2 H azyryna |
||||||||||||
| Formuła molekularna | C 2 H 3 N | ||||||||||||
| Zewnętrzne identyfikatory / bazy danych | |||||||||||||
| |||||||||||||
| nieruchomości | |||||||||||||
| Masa cząsteczkowa | 41,05 g mol -1 | ||||||||||||
| instrukcje bezpieczeństwa | |||||||||||||
| |||||||||||||
| O ile to możliwe i zwyczajowe, stosuje się jednostki SI . O ile nie zaznaczono inaczej, podane dane dotyczą warunków standardowych . | |||||||||||||
Azyryna , dokładniej 2 H -azirine jest najprostszy nienasycony azot - zawierający trzy - członowy heterocykl . Należy do heterocyklicznych układów macierzystych i do klasy substancji cyklicznych imin . Nasyconym analogiem jest azyrydyna , analogiem karbocyklicznym jest cyklopropen . Izomerycznej 1 H -azirine, co prowadzi do proton przy atomie azotu, nie jest stabilny i izomeryzuje do 2 H -azirine.
Produkcja
Preparat 2H- azyryny można otrzymać z azydku winylu pod zmniejszonym ciśnieniem i podwyższoną temperaturą. Acetonitryl i ketenimina powstają jako produkty uboczne .
nieruchomości
Maksimum absorpcji w pentanu w ultrafioletowym zakresie przy długości fali z X = 229 nm .
Azyryna kation jest najmniejsza heterocykliczny aromatyczny związek.
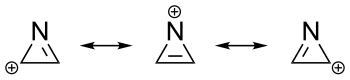
Reakcje
Azyryna jest bardzo reaktywna ze względu na wysokie napięcie pierścienia . Reaguje z elektrofilami i nukleofilami z otwarciem pierścienia.
Pochodne azyryny powstają jako związki pośrednie w przegrupowaniu Nebera .
Indywidualne dowody
- ↑ Substancja ta albo nie została jeszcze sklasyfikowana pod względem niebezpieczeństwa, albo nie znaleziono jeszcze wiarygodnego i możliwego do cytowania źródła.
- ↑ a b J.-C. Guillemin, J.-M. Denis, M.-C. Lasne, J.-L. Ripoll w: Tetrahedron 1988, 44 (14), 4447-4456. doi : 10.1016 / S0040-4020 (01) 86146-9

