Nikotyna
| Formuła strukturalna | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Naturalna substancja nikotyna | ||||||||||||||||||||||
| Generał | ||||||||||||||||||||||
| Nazwisko | Nikotyna | |||||||||||||||||||||
| inne nazwy |
|
|||||||||||||||||||||
| Formuła molekularna | C 10 H 14 N 2 | |||||||||||||||||||||
| Krótki opis |
bezbarwna do brązowawej oleista ciecz o zapachu tytoniu ( pirydyny ) like |
|||||||||||||||||||||
| Identyfikatory zewnętrzne / bazy danych | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Informacje o narkotykach | ||||||||||||||||||||||
| Kod ATC | ||||||||||||||||||||||
| Klasa leków |
Środki do rzucania palenia |
|||||||||||||||||||||
| nieruchomości | ||||||||||||||||||||||
| Masa cząsteczkowa | 162,23 g mol- 1 | |||||||||||||||||||||
| Stan fizyczny |
ciekły |
|||||||||||||||||||||
| gęstość |
1,01 g cm- 3 |
|||||||||||||||||||||
| Temperatura topnienia |
-79 °C |
|||||||||||||||||||||
| temperatura wrzenia |
246°C |
|||||||||||||||||||||
| Ciśnienie pary |
5,6 Pa (20 ° C) |
|||||||||||||||||||||
| Wartość p K S |
|
|||||||||||||||||||||
| rozpuszczalność |
łatwo rozpuszczalny w wodzie , etanolu , eterze dietylowym i chloroformie , mieszalny z wieloma rozpuszczalnikami organicznymi |
|||||||||||||||||||||
| Współczynnik załamania światła |
1,5282 (20°C) |
|||||||||||||||||||||
| instrukcje bezpieczeństwa | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
Szwajcaria: 0,07 ml m- 3 lub 0,5 mg m- 3 − |
|||||||||||||||||||||
| Dane toksykologiczne | ||||||||||||||||||||||
| W miarę możliwości i zwyczajowo stosowane są jednostki SI . O ile nie zaznaczono inaczej, podane dane dotyczą warunków standardowych . Współczynnik załamania: linia Na-D , 20 ° C | ||||||||||||||||||||||
Nikotyna , znany również jako nikotyny , jest alkaloidem naturalnie występujące w liściach rośliny tytoniu , a w mniejszym stopniu innych psiankowatych roślin , które stymulujących lub paraliżujący wpływ na zwojach na autonomiczny układ nerwowy . Pochodne nikotyny rzadko określa się mianem nikotynoidów ; chodzi głównie o syntetyczne neonikotynoidy stosowane jako insektycydy .
Nikotyna jest psychoaktywnym składnikiem z. B. Papierosy są powszechnym narkotykiem ludowym (patrz palenie ).
historia
Tytoń był rytualnie spożywany w Ameryce przez Majów najpóźniej od X wieku. W 1492 roku Krzysztof Kolumb otrzymał suszony tytoń, kiedy przybył do Nowego Świata . Ambasador Francji w Portugalii, Jean Nicot de Villemain, wysłał w 1560 roku nasiona Nicotiana tabacum do króla francuskiego, promując ich zastosowanie lecznicze. Nikotyna została po raz pierwszy wyizolowana pod nazwą Nicotianin w 1828 roku przez chemika Karla Ludwiga Reimanna i lekarza Christiana Wilhelma Posselta w ramach konkursu na Uniwersytecie w Heidelbergu ; wybrali nazwę po Jean Nicot. Struktura chemiczna została wyjaśniona przez Adolfa Pinnera i Richarda Wolffensteina . W 1851 roku belgijski chemik Jean Servais Stas udowodnił, że Hippolyte Visart de Bocarmé otruł swoją ofiarę Gustave'a Fougniesa nikotyną.
Występowanie
Naturalne występowanie
Nikotyna jest produkowana głównie jako metabolit wtórny w znacznych ilościach przez różne gatunki z rodzaju Nicotiana (zwłaszcza Nicotiana tabacum i Nicotiana rustica ) oraz inne rodzaje rodziny psiankowatych (np. Duboisia hopwoodii i Asclepias syriaca ) . Nikotyna została również znaleziona w bardzo niskich stężeniach w niektórych innych gatunkach tej rodziny i blisko spokrewnionej rodzinie powój . Poza tymi rodzinami substancja występuje sporadycznie w niższych stężeniach, np. w rodzaju Erythroxylum z rodziny sekwojów . Nikotyna występuje również w mniejszych ilościach w różnych roślinach psiankowatych, takich jak ziemniaki , pomidory i bakłażany . Ponieważ nikotyna powstaje prawie wyłącznie w korzeniach rośliny tytoniu, tytoń bez nikotyny może być wytwarzany z roślin tytoniu, które zostały zaszczepione na korzeniach roślin pomidora .
Zawartość nikotyny w wyrobach tytoniowych i substytutach
Zawartość nikotyny w dymie papierosowym mierzy się w znormalizowanej maszynie do palenia około 0,6 do 2,4 miligramów , z czego 0,9 do 1,2 mg jest spożywane przez palacza . Zawartość nikotyny w suszu tytoniowym wynosi 0,6 do 2,9% suchej masy . Należy jednak zauważyć, że wskazanie ilości nikotyny na papieros ma bardzo ograniczoną jakość informacyjną, ponieważ zawartość spożytej nikotyny zmienia się w zależności od rodzaju inhalacji i budowy papierosa. Co więcej, ważne jest, aby palacz niekoniecznie spożywał mniej nikotyny dziennie, przechodząc na papierosy o obniżonej zawartości nikotyny, ponieważ wielu palaczy ciągnie je coraz dłużej. Sam papieros zawiera znacznie więcej nikotyny (ok. 12 mg, patrz rozdział dotyczący efektów toksycznych ), która jednak podczas palenia po prostu pali się w większości przed wdychaniem.
Typowy plaster nikotynowy uwalnia około jednego miligrama nikotyny na godzinę w ciągu 16 lub 24 godzin.
Tabaka może być codziennie Nicotinaufnahmemenge podobny do wyniku ciężkiego palacz (20 do 60 mg).
nieruchomości
Fitochemikalia konstytutywne
Nicotiana , łacińska nazwa rodzaju tytoniu , produkuje nikotynę w swoich korzeniach. Gdy roślina dojrzeje, substancja migruje do liści, gdzie osiąga ułamek masowy od 0,5 do 7,5 proc. Nikotynę stosuje się w częściach roślin, zwłaszcza w liściach, w celu odstraszenia drapieżników roślin , pod warunkiem, że drapieżnik posiada układ nerwowy z receptorem nikotynowym acetylocholiny . Nikotyna i nikotynoidy są silnymi insektycydami .
Właściwości fizyczne
Czysta nikotyna jest bezbarwną, oleistą cieczą w temperaturze pokojowej, która szybko brązowieje pod wpływem powietrza. Jest bazą rozpuszczalną w wodzie i lotną w parze wodnej.
| Enancjomery nikotyny | ||
| Nazwisko | ( S ) nikotyna | ( R ) nikotyna |
| inne nazwy |
L- nikotyna (-) - nikotyna |
D- nikotyna (+) - pseudonikotyna nikotynowa |
| Formuła strukturalna |  |
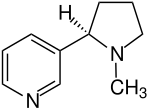
|
| numer CAS | 54-11-5 | 25162-00-9 |
| 22083-74-5 (mieszanina izomerów) | ||
| Numer WE | 686-240-2 | |
| 623-834-2 (mieszanina izomerów) | ||
| Karta informacyjna ECHA | 100.211.968 | |
| 100.152.478 (mieszanina izomerów) | ||
| PubChem | 89594 | 157672 |
| 942 (mieszanina izomerów) | ||
| Wikidane | Q28086552 | Q27119762 |
| Q12144 (mieszanina izomerów) | ||
Właściwości chemiczne
Chemiczną strukturę nikotyny, która opiera się na dwóch połączonych pierścieniach utworzonych z pirydyny i pirolidyny , wyjaśnili Adolf Pinner i Richard Wolffenstein . Nikotyna ma centrum stereogeniczne , jest chiralna . W naturze występuje tylko ( S )-nikotyna. Naturalna nikotyna jest w tej samej konfiguracji co L- prolina w centrum chiralności . Enancjomer ( R ) -nicotine ma patofizjologicznego znaczenia. Ilekroć w tym artykule użyto terminu „nikotyna”, zawsze oznacza ono ( S )-nikotynę.
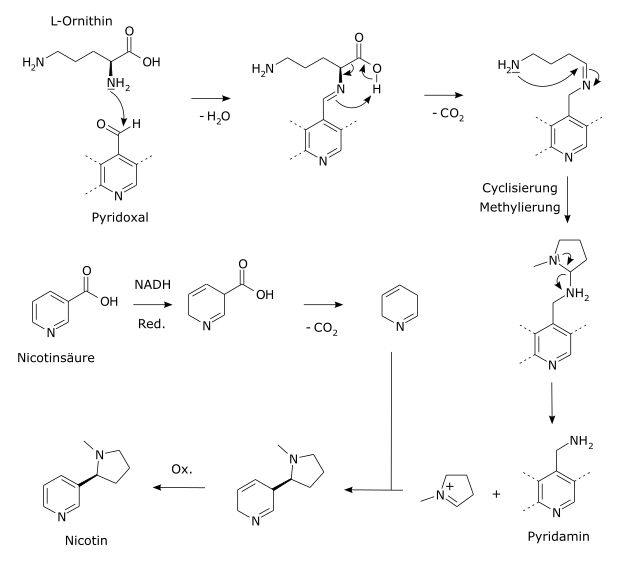
biosynteza
W tytoniu nikotyna jest syntetyzowana z kwasu nikotynowego i L- ornityny w następujących etapach:
- 1,4-Redukcja pierścienia pirydynowego kwasu nikotynowego do kwasu 1,4-dihydronikotynowego przy użyciu NADPH jako środka redukującego.
- Dekarboksylacja kwasu 1,4-dihydronikotynowego do 1,2-dihydropirydyny .
Równolegle:
- Powstawanie putrescyny z L- ornityny.
- Synteza kationu N- metylopirolinium z putrescyny.
Reakcja na gotową nikotynę:
Kwas 1,4-dihydronikotynowy (enamina) reaguje z kationem N- metylopiroliniowy (jonem iminowym) poprzez produkt pośredni, a następnie ponowne utlenianie pierścienia dihydropirydynowego za pomocą NADP + z wytworzeniem nikotyny.
Analityka
Wiarygodne jakościowe i ilościowe oznaczanie nikotyny w różnych materiałach testowych jest możliwe po odpowiednim przygotowaniu próbki poprzez sprzężenie chromatografii gazowej lub HPLC ze spektrometrią mas . W szczególnych przypadkach stosuje się również technikę headspace .
Znaczenie i działanie biochemiczne
Wchłanianie nikotyny przebiega różnie w zależności od wartości pH. Tytoń cygarowy jest wytwarzany z liści, które są zbierane, gdy nie są w pełni dojrzałe. W rezultacie węglowodany w liściach są w dużej mierze rozkładane podczas suszenia i fermentacji, tak że w dymie obecne są głównie produkty rozkładu zasadowych białek. Dym z cygar ma zatem zwykle wartość pH 8,0–8,6. Z drugiej strony w tytoniu papierosowym nikotyna występuje częściowo w postaci protonowanej w postaci związanej z solą, przy pH dymu w zakresie od 6,3 do 5,6. Wchłanianie wolnej nikotyny z dymu alkalicznego odbywa się dobrze przez błony śluzowe. Około 2–5% nikotyny zawartej w tytoniu jest wchłaniane. Dla fizjologicznego działania nikotyny z kwaśnego dymu papierosowego przeznaczonego przez palacza konieczna jest jednak inhalacja, przy czym w organizmie pozostaje około 10-20% nikotyny zawartej w głównym strumieniu dymu. Dostaje się do mózgu ze stosunkowo dużą szybkością napływu od 10 do 20 sekund po inhalacji. Tam nikotyna działa stymulująco na nikotynowe receptory acetylocholiny. Ten typ receptorów znaleziono w przywspółczulnego zwojów , współczulnego zwojów w rdzeniu nadnercza , ośrodkowym układzie nerwowym, jak i na płytach montażowych mechanicznych . Nikotyna aktywuje przywspółczulne nerwy i hamuje współczulne nerwy w swojej działalności. Ponadto nikotyna wspomaga uwalnianie hormonu adrenaliny oraz neuroprzekaźników dopaminy i serotoniny . W niewielkich ilościach nikotyna działa pobudzająco. Nikotyna krótko i odwracalnie przyspiesza bicie serca i powoduje ucisk za. obwodowe naczynia krwionośne; prowadzi to do wzrostu ciśnienia krwi , lekkiej potliwości (spadek odporności skóry ) oraz w wyniku zwężenia naczyń obwodowych, obniżenia temperatury skóry. Do głównych efektów należą przede wszystkim wzrost sprawności psychomotorycznej, a także zdolności uwagi i pamięci oraz relaksacja w niektórych negatywnych stanach afektywnych. Jednak wzrost ten występuje tylko w czasie trwania działania. Spożywanie nikotyny zmniejsza apetyt. Następuje wzrost produkcji soku żołądkowego z powodu uwalniania histaminy i zwiększonej aktywności jelit. Ponadto wiadomo, że nikotyna ma również działanie antydiuretyczne . Wpływ nikotyny i uwalnianie dopaminy powoduje wzrost zachowań konsumenckich, co może skutkować uzależnieniem od nikotyny. Objawy odstawienia, takie jak drażliwość lub nastroje dysforyczne, mogą trwać do 72 godzin. W zdrowych komórkach nikotyna aktywuje kinazę białkową B , która kontroluje metabolizm , wzrost i śmierć komórek. Zwiększa to przeżywalność komórek.
Nikotyna nie znajduje się na liście dopingowej , chociaż zwiększa wytrzymałość.
Zgodnie z kryteriami badania podłużnego, badania związane z przemysłem tytoniowym doprowadziły do wniosku, że nikotyna ma korzystny i ochronny wpływ na chorobę Alzheimera , podczas gdy inne publikacje nie wskazują jej i identyfikują ją jako czynnik ryzyka . W innych badaniach udokumentowano jednak pozytywny wpływ nikotyny na rozwój i terapię choroby. Spożywanie nikotyny wiąże się z mniejszym prawdopodobieństwem rozwoju choroby Parkinsona. U szczurów laboratoryjnych albinosów szkodliwy wpływ na zarodki podczas ciąży wykazywała sól nikotyny (dwuwinian nikotyny), która epigenetycznie objawiała się jako astma w następnym i przedostatnim pokoleniu . Nie wiadomo, czy taki efekt występuje u ludzi. Nikotyna i niektóre jej metabolity są badane w leczeniu choroby Parkinsona i depresji u osób niepalących.
Farmakokinetyka i interakcje farmakokinetyczne
Okres półtrwania nikotyny w osoczu wynosi 1-2 godziny. 10% nikotyny jest wydalane w postaci niezmienionej przez nerki. Reszta jest metabolizowana głównie przez CYP2A6 do kotyniny, która jest częściowo wydalana, a częściowo dalej metabolizowana ze znacznie dłuższym okresem półtrwania w osoczu.
Wielopierścieniowe aromatyczne węglowodany w dymie papierosowym i smole tytoniowej indukują aktywność cytochromu CYP1A2 i CYP2B6, co przyspiesza rozkład substratów CYP1A2. CYP1A2 bierze udział w metabolizmie oksydacyjnym wielu leków i toksyn środowiskowych oraz przyspiesza ich rozkład, w wyniku czego nie można osiągnąć lub utrzymać terapeutycznie pożądanych poziomów farmaceutyków w osoczu. Dotyczy to między innymi niektórych leków psychotropowych i antydepresyjnych. Ponieważ efekt ten nie jest spowodowany nikotyną, nie ma na niego wpływu nikotynowa terapia zastępcza. Nikotyna jest podzielone w organizmie w kotyninę , nikotyna N 'tlenek , nornikotynę , hydroxynicotine i jest w diecie .
Inne toksyny, które działają na receptory acetylocholiny są anatoxin-a niektóre cyjanobakterii , Conine w cętki cykuty , arekoliny z orzechów betel , cytyzyny w Laburnum i epibatydyna z trucizną dwubarwny .
Efekt toksyczny
W małych dawkach nikotyna jest przede wszystkim środkiem pobudzającym . Natomiast w średniej dawce działa odprężająco. Zjawisko zależnej od dawki zmiany efektu zostało opisane jako paradoks Nesbitta . Nikotyna jest tylko bardzo toksyczne dla zwierząt wyższych w wysokich stężeniach , ponieważ w dużych dawkach bloków zwojów na autonomiczny układ nerwowy . Nikotyna jest aktywnym składnikiem tytoniu, który jest głównie odpowiedzialny za uzależniający potencjał konsumpcji tytoniu. Ostre przedawkowanie wiąże się z nudnościami i wymiotami.
W nerkach pod wpływem nikotyny wzrasta ciśnienie krwi, czemu towarzyszy zmniejszony współczynnik filtracji kłębuszkowej i miejscowy przepływ osocza krwi. U młodzieży, nikotyna może prowadzić do zmian w rozwoju jądrze półleżącym , środkowa kora przedczołowa , podstawnoboczne ciała migdałowatego The nucleus łóżko z terminalis Stria, a zakrętu zębatego .
Szybkość wchłaniania nikotyny przez ludzką skórę jest na ogół powolna i zależy od rozpuszczalnika. Czysta zasada (100% nikotyny) jest pobierana bardzo powoli z szybkością 82 µg/cm² na godzinę; H. jeśli nałożysz czystą nikotynę na 10 cm² skóry, połykasz 0,8 mg na godzinę (co w przybliżeniu odpowiada wypaleniu pół papierosa). Przy zastosowaniu 20-procentowego roztworu nikotyny w roztworze alkoholowym na 10 cm² wchłanianie wynosi 0,1 mg nikotyny na godzinę. W rozcieńczonym roztworze wodnym (20 procent) wchłanianie nikotyny jest znacznie szybsze przy 8,8 mg na godzinę.
Przez długi czas zakładano, że nawet w przypadku połknięcia 60 mg nikotyny osobie dorosłej grozi śmierć. Założenie to oparto na wynikach badań toksykologa i farmakologa Rudolfa Koberta. W 1906 opublikował Textbook of Intoxications , w którym oparł się na wynikach eksperymentalnych od 2 do 4 mg i wywnioskował z tego, że maksymalna śmiertelna doustna dawka nikotyny nie może być wyższa niż 60 mg. Kobert prześledził swoje badania wstecz do własnych eksperymentów austriackiego lekarza Karla Damiana von Schroffa w 1856 roku. W 2014 roku farmakolog Bernd Mayer z Uniwersytetu Karla-Franzensa w Grazu skorygował wartość do ponad 500 mg.
W przypadku połykania papierosów przez dzieci, amerykańskie 4-letnie badanie obejmujące 700 przeanalizowanych przypadków wykazało, że przebieg choroby był zawsze łatwy przy połknięciu maksymalnie dwóch papierosów. Dlatego Szwajcarskie Centrum Informacji Toksykologicznej zaleca, aby dzieci konsultowały się z lekarzem tylko w przypadku połknięcia więcej niż dwóch papierosów lub wystąpienia objawów zatrucia (takich jak wymioty, zaczerwienienie skóry, bladość, niepokój). W niektórych przypadkach konsultacja lekarska jest jednak uważana za obowiązkową nawet przy mniejszych ilościach.
Informacje o zawartości nikotyny i substancji smolistych nie mogą już być podawane na opakowaniu paczki papierosów, ponieważ informacje te okazały się mylące. Konsumenci mogą zakładać, że dokonany przez nich wybór jest zdrowszy w porównaniu. Opakowania mają być zaopatrzone w ostrzeżenia zgodnie ze ścisłymi specyfikacjami. Górna granica ilości nikotyny dostarczanej przez dym jest ograniczona do 1 miligrama, ilości smoły do 10 miligramów i ilości CO do 10 miligramów na papieros zgodnie z dyrektywą UE 2014/40. Tytoń w papierosie zawiera średnio około 12 miligramów nikotyny.
Zgodnie z sugestią holenderskiego organu ds. chemikaliów klasyfikacja chemiczna nikotyny została zweryfikowana w 2015 roku. Komitet ds. Oceny Ryzyka (RAC) Europejskiej Agencji Chemikaliów (ECHA) 10 września 2015 r. zmienił klasyfikację nikotyny w następujący sposób: Zarówno doustna, jak i skórna oraz inhalacyjna są sklasyfikowane jako toksyczność 2 w kategorii ostrej rozszerzonej na ostrzeżenia na H300 , H310 i H330 (połknięcie, kontakt ze skórą i inhalacja grozi śmiercią) oraz H411 (Aquatic Chronic 2). Ta klasyfikacja RAC została następnie zaimplementowana przez Komisję Europejską w obowiązującym prawie, co musi być brane pod uwagę przez firmy i urzędy od 1 maja 2020 r.
Skutki rakotwórcze
Nikotyna nie jest na liście rakotwórczych substancji w Światowej Organizacji Zdrowia Międzynarodową Agencję Badań nad Rakiem .
Efekt promujący raka
US Journal of Clinical Investigation donosi, że nikotyna jako część chemioterapii blokuje zdolność organizmu do niszczenia komórek z uszkodzonym materiałem genetycznym. Takie komórki muszą jednak zostać jak najszybciej rozłożone przez organizm podczas takiej terapii, ponieważ w przeciwnym razie guzy nowotworowe już w organizmie będą się dalej rozmnażać z mniejszą przeszkodą. W zdrowych komórkach nikotyna aktywuje kinazę białkową B. Zwiększa to przeżywalność komórek, co w zasadzie jest korzystne, ale szkodliwe, jeśli później zmutują do komórek rakowych. Ponadto doniesiono, że nikotyna sprzyja tworzeniu nowych naczyń krwionośnych ( angiogeneza ), dzięki czemu wszelkie istniejące guzy nowotworowe są lepiej zaopatrzone w składniki odżywcze i mogą szybciej rosnąć.
Potencjał zależności

Nikotyna jest głównie odpowiedzialna za uzależnienie od wyrobów tytoniowych . Uzależniające działanie nikotyny potęgują zawarte w dymie tytoniowym inhibitory monoaminooksydazy . Porównania badań na zwierzętach i badań nad używaniem narkotyków przez ludzi pokazują, że czysta nikotyna jest bardzo uzależniająca, podczas gdy tytoniowy dym papierosowy jest bardzo uzależniający. Lewin odniósł się do tego faktu w Phantastica już w 1924 roku. W połączeniu z innymi substancjami zawartymi w dymie tytoniowym, nikotyna ma niezwykle wysoki potencjał uzależniający i może bardzo szybko doprowadzić do uzależnienia . Według artykułu opublikowanego w 2007 roku przez Davida Nutta i in. Potencjał uzależniający od dymu tytoniowego leży gdzieś pomiędzy alkoholem a kokainą. Dokładniej, potencjał uzależnienia fizycznego dotyczy alkoholu lub barbituranów, a potencjał uzależnienia psychicznego dotyczy kokainy. Porównanie z uzależnieniem od opiatów, takich jak heroina, nie jest wskazane, ponieważ jest to znacznie bardziej skomplikowane w leczeniu, a objawy odstawienia są bardziej nasilone. Wystarczy kilka papierosów lub kilka dni z małym spożyciem papierosów, aby stać się fizycznie zależnym. Potencjał uzależniający nikotyny przyjmowanej doustnie jest znacznie niższy, plastry prawie nie mają potencjału uzależniającego.
Połączenie z użyciem innych substancji
W doświadczeniach na zwierzętach stosunkowo łatwo jest określić, czy spożycie jednej substancji zwiększa późniejszą atrakcyjność innej substancji. Jednak na ludziach, gdy takie bezpośrednie eksperymenty nie są możliwe, można przeprowadzić badania podłużne w celu ustalenia, czy prawdopodobieństwo użycia substancji jest związane z wcześniejszym stosowaniem innych substancji.
U myszy nikotyna zwiększała prawdopodobieństwo późniejszego zażywania kokainy , a eksperymenty pozwoliły na wyciągnięcie konkretnych wniosków na temat podstawowych zmian molekularnych w mózgu. Odcisk biologiczny u myszy odpowiadał zatem obserwacjom epidemiologicznym, że spożywanie nikotyny przez ludzi wiąże się z późniejszym zwiększonym prawdopodobieństwem używania konopi indyjskich i kokainy.
U szczurów etanolowy roztwór konopi zwiększył późniejsze samopodawanie soli nikotyny w dalszych eksperymentach. Badanie zażywania narkotyków wśród około 14 500 uczniów klas dwunastych wykazało, że spożywanie alkoholu wiązało się ze zwiększonym prawdopodobieństwem późniejszego używania tytoniu, konopi i innych nielegalnych substancji.
posługiwać się
Zastosowanie medyczne
Nikotyna stosowana jest w terapii rzucania palenia w postaci plastrów, sprayów czy gumy do żucia. Dostarczona nikotyna zmniejsza objawy odstawienia, gdy nie palisz; wielu zagrożeń stwarzanych przez dym tytoniowy można uniknąć, stosując czystą nikotynę.
Metaanaliza 103 randomizowanych, kontrolowanych placebo badań wykazała, że prawdopodobieństwo nawrotu palenia wśród palaczy, którzy rzucili palenie bez pomocy, wynosi 97 procent w ciągu sześciu miesięcy od rzucenia palenia. Do 2012 roku zakładano, że preparaty zastępujące nikotynę, przy odpowiednim dawkowaniu i dalszym profesjonalnym wskazówkach, mogą zwiększyć szanse powodzenia o trzy procent. Niedawne badanie z 2012 r. wykazało, że odsetek nawrotów wśród osób, które stosowały substytuty nikotyny w celu rzucenia palenia, był tak samo wysoki, jak tych, którzy rzucili palenie bez pomocy.
Zaktualizowany przegląd dokonany przez Cochrane Collaboration w październiku 2020 r. potwierdził, że stosowanie zawierających nikotynę papierosów elektronicznych wyraźnie przewyższa wszystkie inne metody skutecznego rzucenia palenia. Dotyczy to zwłaszcza nikotynowych gum do żucia i plastrów. Stwierdzono jeszcze wyraźniejszą przewagę w porównaniu ze środkami wsparcia behawioralnego lub próbami rzucenia palenia bez żadnego wsparcia.
Gumy do żucia zawierające nikotynę zwykle zawierają 2 mg nikotyny dla palaczy z umiarkowanym spożyciem tytoniu lub 4 mg dla osób silnie uzależnionych. W Niemczech są dostępne tylko w aptekach. W Szwajcarii wszystkie leki na zaprzestanie palenia nikotyny należą do kategorii D, więc są dostępne w aptekach i drogeriach.
W odniesieniu do szczepionek sprzężonych z nikotyną w celu wytworzenia przeciwciała anty-nikotyny przeciwciał są podobne badania. Ponadto badani są antagoniści nikotynowego receptora acetylocholiny do odstawiania od piersi.
Zastosowanie w ochronie roślin
Czysta nikotyna była wcześniej stosowana w ochronie upraw jako pestycyd przeciwko owadom ssącym lub gryzącym (w tym mszycom ). Substancja jest dobrze tolerowana przez rośliny, a także łatwo biodegradowalna. Jednak ze względu na od dawna nieprawdziwe informacje o wysokiej toksyczności, nikotyna została zabroniona od lat 70. XX wieku. Jako substytut zastosowano syntetyczne insektycydy na bazie organofosforanów, takie jak E605 . Inne naturalne nikotynoidy i syntetyczne neonikotynoidy są opracowywane jako insektycydy głównie do użytku komercyjnego.
Aplikacja w e-papierosie
Nikotyna jest również stosowana jako opcjonalny składnik e-papierosa .
Nazwy handlowe
Nicopatch (A), Nicorette (D, A, CH), Nicotinell (D, A, CH), Nicotrol (A), Nikaloz (A), Nikofrenon (D), NiQuitin (D, A)
literatura
- Helmut Schievelbein (red.): Nikotyna - Farmakologia i toksykologia dymu tytoniowego . Thieme Verlag, Stuttgart 1968, DNB 457705825 .
linki internetowe
Indywidualne dowody
- ↑ b c d e f g wejście na nikotynę w bazie substancji GESTIS o w IFA , do których dostęp 8 stycznia 2020 r. (wymagany JavaScript)
- ↑ a b c d AC Moffat (red.): Izolacja Clarke'a i identyfikacja narkotyków. Wydanie II. The Pharmaceutical Press, Londyn 1986, ISBN 0-85369-166-5 , str. 807-808.
- ^ Wpis dotyczący nikotyny. W: Rompp Online . Georg Thieme Verlag, dostęp 12 kwietnia 2011 r.
- ↑ David R. Lide (red.): CRC Handbook of Chemistry and Physics . Wydanie 90. (Wersja internetowa: 2010), CRC Press / Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, s. 3-386.
- ↑ Wpis na nikotyny w wykazie klasyfikacji i oznakowania w Europejskiej Agencji Chemikaliów (ECHA), dostępne w dniu 1 lutego 2016 roku producenci lub dystrybutorzy mogą rozwinąć się zharmonizowanej klasyfikacji i oznakowania .
- ↑ Swiss Accident Insurance Fund (Suva): Wartości limitów - aktualne wartości MAK i BAT (szukaj 54-11-5 lub nikotyna ), dostęp 28 sierpnia 2020 r.
- ↑ a b c d Wpis dotyczący nikotyny w bazie danych ChemIDplus Narodowej Biblioteki Medycznej Stanów Zjednoczonych (NLM), dostęp 28 sierpnia 2020 r.
- ^ Doris Schwarzmann-Schafhauser: Nikotyna. W: Werner E. Gerabek , Bernhard D. Haage, Gundolf Keil , Wolfgang Wegner (red.): Enzyklopädie Mediizingeschichte. De Gruyter, Berlin / Nowy Jork 2005, ISBN 3-11-015714-4 , s. 1053.
- ↑ a b c Izuru Yamamoto, John E. Casida (red.): Insektycydy nikotynowe i nikotynowy receptor acetylocholiny . Springera, 1999.
- ^ Wpis dotyczący neonikotynoidów. W: Rompp Online . Georg Thieme Verlag, dostęp 11 września 2013 r.
- ^ B Dietrich Hoffmann Ilse Hoffmann: Chemistry and Toxicology . (PDF). W: Monografia Kontroli Palenia i Tytoniu Nr. 9 - Cygara: skutki zdrowotne i trendy. Rozdział 3, Narodowy Instytut Raka, 1998.
- ^ HP Rang i wsp.: Farmakologia Rang i Dale'a. Wydanie szóste. Elsevier, 2007, ISBN 978-0-7020-4074-0 , s. 598.
- ^ Robert L. Metcalf: Kontrola owadów. W: Encyklopedia chemii przemysłowej Ullmanna . Wydanie siódme. Wiley 2007, s. 9.
- ↑ Eckart Eich: Alkaloidy pochodzące z ornityny. W: Solanaceae i Convolvulaceae: Metabolity wtórne - biosynteza, chemotaksonomia, znaczenie biologiczne i ekonomiczne (podręcznik). Springer Verlag, 2008, ISBN 978-3-540-74540-2 , s. 33-188.
- ^ Zawartość nikotyny we wspólnych warzywach . W: The New England Journal of Medicine . taśma 329 , sierpień 1993, s. 437 , doi : 10.1056/NEJM199308053290619 .
- ^ Rainer Tölle, Gerhard Buchkremer: Palenie papierosów: epidemiologia, psychologia, farmakologia i terapia. Wydanie drugie, Springer, 2013. ISBN 978-3-642-74044-2 . str. 45.
- ^ Rainer Tölle, Gerhard Buchkremer: Palenie papierosów: epidemiologia, psychologia, farmakologia i terapia. Wydanie drugie, Springer, 2013. ISBN 978-3-642-74044-2 . str. 36.
- ^ Alfred Lichtenschopf: Standardy odstawienia tytoniu: Konsensus Austriackiego Towarzystwa Pneumologicznego - Aktualizacja 2010. Springer-Verlag, 2012, ISBN 978-3-7091-0979-3 , s. 55.
- ↑ O działaniu tabaki , doi: 10.1007 / BF01865916 .
- ↑ Tytoń (tytoń w liściach). Serwis informacji o transporcie, dostęp 13 sierpnia 2017 r .
- ↑ A. Pinner, R. Wolffenstein: O nikotynie. W: Sprawozdania Niemieckiego Towarzystwa Chemicznego. 24, 1891, s. 61-67, doi: 10.1002 / cber.18910240108 .
- ↑ A. Pinner, R. Wolffenstein: O nikotynie. W: Sprawozdania Niemieckiego Towarzystwa Chemicznego. 24, 1891, s. 1373-1377, doi: 10.1002/cber.189102401242 .
- ↑ A. Pinner, R. Wolffenstein: O nikotynie. W: Sprawozdania Niemieckiego Towarzystwa Chemicznego. 25, 1892, s. 1428-1433, doi: 10.1002 / cber.189202501214 .
- ^ Paul M. Dewick: Naturalne produkty lecznicze: podejście biosyntetyczne . Wydanie II. Wiley-Blackwell, 2001, s. 313.
- ↑ Xuewen Wang, Jeffrey L. Bennetzen: Aktualny stan i perspektywy badań nad genomiką, genetyką i genami biosyntezy nikotyny w Nicotiana. W: Genetyka Molekularna i Genomika. 290, 2015, s. 11, doi: 10.1007 / s00438-015-0989-7 . PMID 25582664 .
- ↑ M. Iwai, T. Ogawa, H. Hattori, K. Zaitsu, A. Ishii, O. Suzuki, H. Seno: Prosta i szybka metoda oznaczania jednoczesnego oznaczania ilościowego nikotyny i kotyniny w moczu przy użyciu mikroekstrakcji za pomocą upakowanego sorbentu i chromatografia gazowa-spektrometria mas. W: Nagoya J Med Sci. 75 (3-4), sierpień 2013, s. 255-261. PMID 24640182 .
- ↑ KB Scheidweiler, DM Shakleya, MA Huestis: Jednoczesna ocena ilościowa nikotyny, kotyniny, trans-3'-hydroksykotyniny, norkotyniny i mekamylaminy w ludzkim moczu metodą chromatografii cieczowej z tandemową spektrometrią mas. W: Clin Chim Acta. 413 (11-12), 14 czerwca 2012, s. 978-984. PMID 22394455 .
- ^ A. Lopes, N. Silva, MR Bronze, J. Ferreira, J. Morais: Analiza metabolitów kokainy i nikotyny w ściekach metodą chromatografii cieczowej tandemowej spektrometrii masowej. Wzory indeksów nadużyć krzyżowych w dużej społeczności W: Sci Total Environ. 487, 15.07.2014, s. 673-680. PMID 24200094 .
- ↑ N. Liachenko, A. Boulamery, N. Simon: Oznaczanie nikotyny i metabolitów w ludzkim osoczu za pomocą ultrasprawnej chromatografii cieczowej-tandemowej spektrometrii masowej: proste podejście do rozwiązywania problemu zanieczyszczenia i zastosowania klinicznego. W: Fundam Clin Pharmacol. 29 (5), październik 2015, s. 499-509. PMID 26118829 .
- ↑ C. Müller, F. Vetter, E. Richter, F. Bracher: Oznaczanie kofeiny, miosminy i nikotyny w czekoladzie metodą mikroekstrakcji fazy stałej z fazą nad roztworem w połączeniu z chromatografią gazową-tandemową spektrometrią mas. W: J Food Sci. 79 (2), luty 2014, s. T251-T255. PMID 24446916 .
- ^ Offermanns S.: Tabakrauch , W: Pharmakologie und Toxikologie. Springer-Lehrbuch (2016), s. 925-929; doi: 10.1007 / 978-3-662-46689-6_72 Springer, Berlin, Heidelberg; ISBN 978-3-662-46688-9 .
- ↑ KD Brunnemann, D. Hoffmann: pH dymu tytoniowego , Food and Cosmetics Toxicology, tom 12, wydanie 1, 1974, str. 115-124, doi: 10.1016 / 0015-6264 (74) 90327-7 .
- ↑ Aschenbrenner, Stahl: Handbuch des Tobakhandel , 6. wydanie 1950, Vlg. Oldenburger Verlagshaus, s. 516 f.
- ↑ J. Le Houezec: Rola farmakokinetyki nikotyny w uzależnieniu od nikotyny i nikotynowej terapii zastępczej: przegląd. W: Int J Tuberc Lung Dis . 7, 2003, s. 811-819. PMID 12971663 .
- ↑ M. Sabha, JE Tanus-Santos, JC Toledo, M. Cittadino, JC Rocha, H. Moreno: Transdermalna nikotyna naśladuje dysfunkcję śródbłonka wywołaną paleniem . W: Farmakologia Kliniczna i Terapeutyka . taśma 68 , nie. 2 , sierpień 2000, s. 167-174 , doi : 10.1067/mcp.2000.108851 , PMID 10976548 .
- ^ F. Scott Hall, Andre Der-Avakian, Thomas J. Gould, Athina Markou, Mohammed Shoaib, Jared W. Young: Negatywne stany afektywne i zaburzenia poznawcze w uzależnieniu od nikotyny. W: Neuroscience & Biobehavioral Reviews. 2015, doi: 10.1016 / j.neubiorev.2015.06.004 . PMID 26054790 .
- ↑ Sybren F. de Kloet, Huibert D. Mansvelder, Taco J. De Vries: Cholinergiczna modulacja szlaków dopaminy przez nikotynowe receptory acetylocholiny. W: Farmakologia biochemiczna. 2015, doi: 10.1016 / j.bcp.2015.07.014 . PMID 26208783 .
- ↑ Otto-Michael Lesch, Henriette Walter: Alkohol i tytoń: medyczne i socjologiczne aspekty używania, nadużywania i uzależnienia. Springer-Verlag, 2009, ISBN 978-3-211-48634-4 , s. 144.
- ↑ T. Mündel, DA Jones: Wpływ przezskórnego podawania nikotyny na wytrzymałość wysiłkową u mężczyzn . W: Fizjologia Eksperymentalna . taśma 91 , nie. 4 , lipiec 2006, s. 705-713 , doi : 10.1113 / expphysiol.2006.033373 , PMID 16627574 .
- ↑ JK Cataldo, JJ Prochaska, SA Glantz: Palenie papierosów jest czynnikiem ryzyka choroby Alzheimera: analiza kontrolująca przynależność do przemysłu tytoniowego. W: Journal of Alzheimer's disease: JAD. Tom 19, Numer 2, 2010, s. 465-480, doi: 10.3233 / JAD-2010-1240 . PMID 20110594 , PMC 2906761 (darmowy pełny tekst).
- ↑ M. Mehta, A. Adem, MS Kahlon, MN Sabbagh: Receptor nikotynowy acetylocholiny: palenie i choroba Alzheimera ponownie. W: Frontiers in Bioscience . 2012, E4, s. 169-180. PMID 22201862 , doi: 10.2741 / 367 .
- ↑ Maryka Quik, Xiomara A. Perez, Tanuja Bordia: Nikotyna jako potencjalny czynnik neuroprotekcyjny w chorobie Parkinsona. W: Zaburzenia ruchowe. 27, 2012, s. 947, doi: 10.1002 / mds.25028 . PMID 22693036 . PMC 3685410 (darmowy pełny tekst).
- ↑ Virender K Rehan, Jie Liu i in.: Okołoporodowa ekspozycja na nikotynę wywołuje astmę u potomstwa drugiego pokolenia. W: BMC Medycyna . 10, 2012, s. 129, doi: 10.1186 / 1741-7015-10-129 .
- ^ B George E. Barreto, Alexander Iarkov Valentina Echeverria Moran: korzystnych efektów nikotynowych, kotyniny i jego metabolitów jako potencjalne środki do choroby Parkinsona. W: Frontiers in Aging Neuroscience. 6, 2015, doi: 10.3389 / fnagi.2014.00340 . PMID 25620929 . PMC 4288130 (wolny pełny tekst).
- ^ YS Mineur, MR Picciotto: Receptory nikotynowe i depresja: powrót do hipotezy cholinergicznej i jej rewizja . W: Trendy Pharmacol. Nauka. taśma 31 , nie. 12 grudnia 2010, s. 580-586 , doi : 10.1016 / j.tips.2010.09.004 , PMID 20965579 , PMC 2991594 (darmowy pełny tekst).
- ^ Offermanns S. „Dym tytoniowy”. W: Pharmakologie und Toxikologie , Springer-Lehrbuch (2016), s. 925-929; doi: 10.1007 / 978-3-662-46689-6_72 Springer, Berlin, Heidelberg; ISBN 978-3-662-46688-9 .
- ↑ Niklaus Spoon: „Interakcje narkotyków z dymem tytoniowym” W: pharma-kritik , tom 35, PK915, artykuł online, doi: 10.37667/pk.2013.915 .
- ↑ AC Parrott: Paradoks Nesbitta rozwiązany? Modulacja stresu i pobudzenia podczas palenia papierosów . W: Uzależnienie . taśma 93 , nie. 1 , styczeń 1998, s. 27-39 , doi : 10.1046/j.1360-0443.1998.931274.x , PMID 9624709 .
- ↑ F. Pistillo, F. Clementi, M. Zoli, C. Gotti: Przekaźnictwo synaptyczne nikotynowe, glutaminergiczne i dopaminergiczne oraz plastyczność w układzie mezokortykolimbicznym: koncentracja na działaniu nikotyny. W: Prog Neurobiol. (2015), Tom 124, s. 1–27. doi: 10.1016 / j.pneurobio.2014.10.002 . PMID 25447802 .
- ↑ Gaurav Jain, Edgar A. Jaimes: Sygnalizacja nikotynowa i progresja przewlekłej choroby nerek u palaczy. W: Farmakologia biochemiczna. 86, 2013, s. 1215, doi: 10.1016 / j.bcp.2013.07.014 . PMID 23892062 . PMC 3838879 (darmowy pełny tekst).
- ^ Robert F. Smith, Craig G. McDonald, Hadley C. Bergstrom, Daniel G. Ehlinger, Jennifer M. Brielmaier: Młodzieżowa nikotyna wywołuje utrzymujące się zmiany w rozwoju łączności nerwowej. W: Neuroscience & Biobehavioral Reviews. 55, 2015, s. 432, doi: 10.1016 / j.neubiorev.2015.05.019 . PMID 26048001 .
- ^ S. Zorin i in.: Test in vitro przepuszczalności nikotyny przez ludzką skórę. Ocena ryzyka i aspekty bezpieczeństwa. (PDF; 194 kB). W: Ann Occup Hyg . 43, 1999, s. 405-413.
- ↑ B. Mayer: Ile nikotyny zabija człowieka? Odniesienie ogólnie przyjętej dawki śmiertelnej do wątpliwych eksperymentów na sobie w dziewiętnastym wieku. W: Archiwum Toksykologii . Tom 88, Numer 1, styczeń 2014, s. 5-7, doi: 10.1007 / s00204-013-1127-0 . PMID 24091634 . PMC 3880486 (darmowy pełny tekst).
- ↑ D. McGee, T. Brabson, J. McCarthy, M. Picciotti: Czteroletni przegląd spożycia papierosów u dzieci . W: Pogotowie ratunkowe dla dzieci . taśma 11 , nie. 1 , 1995, s. 13-16 , doi : 10.1097/00006565-199502000-00004 .
- ↑ Papierosy niebezpieczne dla małych dzieci? Szwajcarskie Centrum Informacji Toksykologicznej.
- ↑ Częste zatrucia nikotyną. (PDF; 41 kB). Wspólne centrum informacji o truciznach.
- ↑ Dyrektywa Parlamentu Europejskiego i Rady 2014/ 40 /UE z dnia 3 kwietnia 2014 r. w sprawie harmonizacji przepisów prawnych i administracyjnych państw członkowskich w sprawie wytwarzania, prezentowania i sprzedaży wyrobów tytoniowych i powiązanych wyrobów oraz uchylenia dyrektywy 2001/37/WE
- ↑ Opinia RAC proponująca zharmonizowaną klasyfikację i oznakowanie nikotyny na poziomie UE. 10 września 2015, udostępniono 30 października 2015.
- ↑ Rozporządzenie (UE) 2018/1480
- ^ Agenci sklasyfikowani w monografiach IARC, tomy 1-107. (PDF; 139 kB). Źródło 27 maja 2013.
- ↑ Nikotyna zatrzymuje chemioterapię . 3 kwietnia 2006, dostęp 8 września 2019 . Wissenschaft.de.
- ↑ Piyali Dasgupta, Rebecca Kinkade, Bharat Joshi, Christina DeCook, Eric Haura, Srikumar Chellappan: Nikotyna hamuje apoptozę indukowaną przez leki chemioterapeutyczne poprzez zwiększenie XIAP i przeżycie . W: PNAS . 103, 2006, s. 6332-6337, doi: 10.1073 / pnas.0509313103 .
- ↑ Wolfram Parzefall, Manfred Neuberger, Rolf Schulte-Hermann: Czynniki rakotwórcze dymu tytoniowego . (PDF; 29 kB). Źródło 27 maja 2013.
- ↑ C. Schaal, SP Chellappan: Proliferacja komórek za pośrednictwem nikotyny i progresja guza w nowotworach związanych z paleniem. W: Badania nad rakiem molekularnym. 12, 2014, s. 14, doi: 10.1158 / 1541-7786.MCR-13-0541 . PMID 24398389 . PMC 3915512 (darmowy pełny tekst).
- ↑ David J Nutt, Leslie A King, Lawrence D Phillips: Szkodliwe działanie narkotyków w Wielkiej Brytanii: wielokryterialna analiza decyzji. W: Lancet. 376, 2010, s. 1558-1565, doi: 10.1016 / S0140-6736 (10) 61462-6 .
- ↑ Toksyczność leków. Rober Gable, dostęp 14 grudnia 2015 .
- ↑ RS Gable: Toksyczność ostra leków a status regulacyjny. W: JM Fish (red.): Narkotyki i społeczeństwo: polityka publiczna USA. Rowman & Littlefield Publishers, Lanham, MD 2006, s. 149-162.
- ↑ Karl Fagerström: Determinanty używania tytoniu i zmiana nazwy FTND na test Fagerströma na uzależnienie od papierosów . W: Badania nad nikotyną i tytoniem . 14, 2012, s. 75-78.
- ^ Anne-Sophie Villégier i in.: Inhibitory monoaminooksydazy umożliwiają lokomotoryczne i nagradzające reakcje na nikotynę . W: Neuropsychofarmakologia . 31, 2006, s. 1704-1713.
- ↑ James D. Belluzzi i wsp.: Aldehyd octowy zwiększa samopodawanie nikotyny u dorastających szczurów . W: Neuropsychofarmakologia. 30, 2005, s. 705-712.
- ^ JE Rose, WA Corrigall: Samopodawanie nikotyny u zwierząt i ludzi: podobieństwa i różnice. W: Psychofarmakologia . 130, 1997, s. 28-40. PMID 9089846 .
- ↑ SCENIHR : Pytania dotyczące dodatków do tytoniu: Czy rozwój uzależnienia od nikotyny jest zależny od dawki? (2010), dostęp 29 lipca 2013.
-
^ L. Lewin: Fantastyka. Odrętwiające i ekscytujące stymulanty. 1924, Vlg. Georg Stilke Berlin, s. 334, przypis 1.
„Istnieją również serie testów, w których pominięto przyzwyczajenie i nawet po dziesięciu czy stu zastrzykach nikotyny te same objawy powtarzały się z taką samą siłą i z taką samą siłą. oczywiście ”. - ↑ Chirurg naczelny (USA): Jak dym tytoniowy powoduje choroby: Biologia i behawioralne podstawy chorób związanych z paleniem: Raport naczelnego chirurga, Uzależnienie od nikotyny: przeszłość i teraźniejszość . 2010, dostęp 29 lipca 2013.
- ↑ D. Nutt i in.: Opracowanie racjonalnej skali do oceny szkodliwości leków o potencjalnym nadużywaniu. (PDF do pobrania przez Researchgate; 127 kB) 2007, dostęp 2 lipca 2020 .
- ↑ Redukcja szkód związanych z uzależnieniem od nikotyny - Pomaganie ludziom, którzy nie mogą rzucić palenia . ( Pamiątka z 29 kwietnia 2016 w Archiwum Internetowym ) (PDF; 1,9 MB). Raport Grupy Doradczej Tytoniu Królewskiego Kolegium Lekarzy, październik 2007, s. 98-99.
- ^ ER Kandel , DB Kandel : Shattuck Wykład: Molekularna podstawa nikotyny jako leku wejściowego. W: The New England Journal of Medicine . Tom 371, numer 10, wrzesień 2014, s. 932-943, doi: 10.1056 / NEJMsa1405092 . PMID 25184865 , PMC 4353486 (darmowy pełny tekst).
- ↑ KM Keyes, A. Hamilton, DB Kandel : Analiza kohort urodzeniowych palenia papierosów wśród młodzieży i późniejszego używania marihuany i kokainy. W: American Journal of Public Health . [Publikacja elektroniczna przed drukiem] kwiecień 2016, doi: 10.2105/AJPH.2016.303128 . PMID 27077359 .
- ↑ LV Panlilio, C. Zanettini, C. Barnes, M. Solinas, SR Goldberg: Wcześniejsza ekspozycja na THC Zwiększa uzależniające działanie nikotyny u szczurów. W: Neuropsychopharmacology: oficjalna publikacja American College of Neuropsychopharmacology. Tom 38, Numer 7, czerwiec 2013, s. 1198–1208, doi: 10.1038 / npp.2013.16 . PMID 23314220 , PMC 3656362 (darmowy pełny tekst).
- ↑ T. Kirby, AE Barry: Alkohol jako narkotyk wejściowy: badanie 12-klasistów z USA. W: The Journal of School Health. Tom 82, Numer 8, sierpień 2012, s. 371-379, doi: 10.1111 / j.1746-1561.2012.00712.x . PMID 22712674 , PDF (dostęp 3 maja 2016 r.).
- ↑ Komisja ds. Narkotyków Niemieckiego Towarzystwa Lekarskiego: Zalecenia dotyczące terapii uzależnienia od tytoniu („Odzwyczajanie się od palenia”) (PDF), Zarządzenie narkotykowe w praktyce, wydanie 2, tom 37, wydanie specjalne 2, listopad 2010 r.
- ^ A. Molyneux: terapia zastępcza nikotyny. W: BMJ . 2004, tom 328, nr 7437, s. 454-456. PMID 14976103 , doi: 10.1136 / bmj.328.7437.454 .
- ↑ Stead i wsp.: Nikotynowa terapia zastępcza w rzucaniu palenia. Cochrane Tobacco Addiction Group, 16 lipca 2008, doi: 10.1002/14651858.CD000146.pub3 .
- ↑ zastąpienie nikotyny i innych leków do zaprzestania palenia . DKFZ, dostęp 6 marca 2013 r.
- ↑ HR Alpert, GN Connolly, L. Biener: Prospektywne badanie kohortowe kwestionujące skuteczność populacyjnej interwencji medycznej w rzucaniu palenia. W: Kontrola tytoniu . Tom 22, numer 1, styczeń 2013, s. 32-37, doi: 10.1136 / tytońcontrol-2011-050129 . PMID 22234781 .
- ↑ Cochrane Niemcy: Przegląd Cochrane pokazuje korzyści płynące z e-papierosów w rzucaniu palenia , 14 października 2020 r.
- ^ EH Cerny, T. Cerny: Szczepionki przeciwko nikotynie. W: Hum Vaccin . 2009, tom 5 (4), s. 200-205. PMID 19276649 .
- ↑ PR Pentel, MG LeSage: Nowe kierunki w projektowaniu i stosowaniu szczepionek nikotynowych. W: Adv Pharmacol. Tom 69, 2014, s. 553-580. doi: 10.1016 / B978-0-12-420118-7.00014-7 . PMID 24484987 ; PMC 4047682 (darmowy pełny tekst).
- ↑ PA Crooks, MT Bardo, LP Dwoskin: Antagoniści receptora nikotynowego w leczeniu nadużywania nikotyny. W: Adv Pharmacol. Tom 69, 2014, s. 513-551. doi: 10.1016 / B978-0-12-420118-7.00013-5 . PMID 24484986 ; PMC 4110698 (darmowy pełny tekst).
- ↑ Steven R. Sims: Kompozycje i procesy owadobójcze . Amerykańskie zgłoszenie patentowe 13/078641.