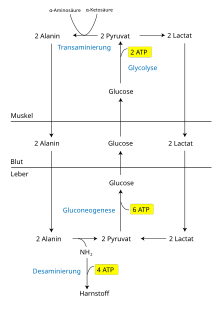
Cykl Coriego
Cykl Cori (nazwa pochodzi od jego odkrywcy, Gerty Cori i Carl Cori ) opisuje cykl glukoza i jego produkty rozpadu między mięśniach szkieletowych i wątrobie . Rozszerzony opis obejmuje szlaki metaboliczne glukoneogenezy , kwasu glutaminowego (Glu), części cyklu kwasu cytrynowego oraz cyklu mocznikowego .
Nawet w warunkach tlenowych mięsień szkieletowy nie jest w stanie przekształcić mleczanu z powrotem w glukozę: brakuje mu enzymów do glukoneogenezy . Z tego powodu dochodzi do obiegu metabolitów między mięśniami a wątrobą – ta ostatnia ma odpowiedni repertuar enzymów . W swojej pierwotnej formie ten cykl organowy nazwano „cyklem Cori” . Rozszerzona forma tego samego, „cykl glukozowo-alaninowy” ma prawdopodobnie większe znaczenie, ponieważ jednocześnie zapobiega zatruciu mięśni amoniakiem, dostarczając go do aparatu detoksykacyjnego wątroby ( cykl mocznikowy ).
Cykl Coriego
Kiedy mięśnie są ćwiczone, w mięśniach szybko pojawia się pewien niedobór tlenu. W tych bardziej beztlenowych warunkach łańcuch oddechowy w mitochondriach ulega spowolnieniu, a energia jest generowana głównie przez glikolizę . Z drugiej strony pirogronian jest mniej rozkładany w cyklu kwasu cytrynowego. Zamiast tego pirogronian reaguje beztlenowo, tworząc kwas mlekowy . NAD + jest regenerowany do glikolizy. Kwas mlekowy jest uwalniany do krwiobiegu w postaci mleczanu - ta ścieżka jest pokazana na rysunku w formie skróconej (patrz pirogronian ). Do wątroby pochłania mleczanu z krwi i przekształca ją z powrotem do glukozy poprzez glukoneogenezy poprzez szczawiooctan . Ta glukoza może – w zależności od aktualnego stanu zaopatrzenia w energię – zostać dostarczona do magazynu energii w wątrobie w postaci glikogenu lub uwolniona do krwiobiegu w celu ponownego zasilenia mięśni.
Należy jednak zauważyć, że nie jest to zamknięty obieg energetyczny. W procesie glukoneogenezy w wątrobie trzeba wydać więcej energii niż w przypadku glikolizy w mięśniach. Jest tak, ponieważ w glukoneogenezie silnie endotermiczną reakcję pirogronianu z fosfoenolopirogronianu (PEP) jest zablokowane w energochłonnym sposób , podczas gdy energia uwolniona w wyniku reakcji egzotermicznej do fruktozo-1,6-BP do fruktozo-6-P lub glukozy 6-P nie jest używany do glukozy. W glukoneogenezie z pirogronianu na każdą cząsteczkę glukozy należy zastosować 4 ATP , 2 GTP i 2 NADH . Jednak w glikolizie z jednej cząsteczki glukozy powstają tylko 2 ATP i 2 NADH.
Cykl glukoza-alanina
W cytozolu białka są rozkładane na aminokwasy . Te z kolei są deaminowane przez transaminację, a pozostała struktura węgla jest wprowadzana do cyklu kwasu cytrynowego . Grupa aminowa aminokwasów jest czasowo przenoszona do kofaktora fosforanu pirydoksalu (PLP) podczas transaminacji ; W ten sposób PLP staje się fosforanem pirydoksaminy (PAMP). Aminotransferazy alaninowej (ALAT ALT) (nazywany także transaminazy glutaminian pirogronianowej GPT) przenosi amino zgrupowanie PAMP pirogronianu w mięśniach. Tworzy to alaninę i zregenerowany PLP, który może następnie zająć nowe grupy aminowe. Alanina jest transportowana przez krew do wątroby, gdzie ALAT zamienia PLP i alaninę w PAMP i pirogronian, które mogą być wykorzystane do glukoneogenezy i są odsyłane z powrotem do komórek pozawątrobowych jako glukoza.
ALAT przenosi grupę aminową z PAMP do α-ketoglutaranu. Powstały glutaminian jest przekształcany w mitochondriach komórki wątroby przez dehydrogenazę glutaminianową (GLDH) do α-ketoglutaranu i NH 3 , ten ostatni jest przekształcany przez syntetazę fosforanu karbamoilu I z CO 2 do fosforanu karbamoilu , który przepływa do cyklu mocznikowego . Drugi NH 2 grupa mocznik jest dostarczany przez produkt transaminacji asparaginianu (Asp), który jest z kolei podzielony na argininę i fumaran . Wreszcie mocznik oddziela się od argininy . Fumaran można zregenerować do asparaginianu poprzez jabłczan i szczawiooctan (cykl asparaginianowy). Mocznik jest wydalany przez nerki .
W przeciwieństwie do cyklu Cori, cykl alaninowy nie tylko regeneruje węglowodany, ale także usuwa z mięśnia NH 3 . W tym celu jednak energia musi być włożony w syntezie mocznika w wątrobie, w celu dysponowania NH 3 .
literatura
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer : Biochemia. 6 wydanie, Spektrum Akademischer Verlag, Heidelberg 2007. ISBN 978-3-8274-1800-5 .
- Donald Voet, Judith G. Voet: Biochemia. Wydanie trzecie, John Wiley & Sons, Nowy Jork 2004. ISBN 0-471-19350-X .