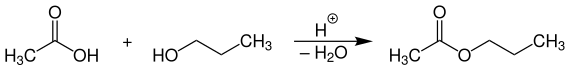Ester n- propylowy kwasu octowego
| Formuła strukturalna | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Generał | ||||||||||||||||||||||
| Nazwisko | Ester n- propylowy kwasu octowego | |||||||||||||||||||||
| inne nazwy |
|
|||||||||||||||||||||
| Formuła molekularna | C 5 H 10 O 2 | |||||||||||||||||||||
| Krótki opis |
lotna, bezbarwna ciecz o owocowym zapachu |
|||||||||||||||||||||
| Zewnętrzne identyfikatory / bazy danych | ||||||||||||||||||||||
| ||||||||||||||||||||||
| nieruchomości | ||||||||||||||||||||||
| Masa cząsteczkowa | 102,13 g mol -1 | |||||||||||||||||||||
| Stan fizyczny |
ciekły |
|||||||||||||||||||||
| gęstość |
0,89 g cm- 3 (20 ° C) |
|||||||||||||||||||||
| Temperatura topnienia |
-95 ° C |
|||||||||||||||||||||
| temperatura wrzenia |
102 ° C |
|||||||||||||||||||||
| Ciśnienie pary |
|
|||||||||||||||||||||
| rozpuszczalność |
|
|||||||||||||||||||||
| Współczynnik załamania światła |
1.3844 |
|||||||||||||||||||||
| instrukcje bezpieczeństwa | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
DFG / Szwajcaria: 100 ml m -3 lub 420 mg m -3 |
|||||||||||||||||||||
| Dane toksykologiczne | ||||||||||||||||||||||
| O ile to możliwe i zwyczajowe, stosuje się jednostki SI . O ile nie zaznaczono inaczej, podane dane dotyczą warunków standardowych . Współczynnik załamania: linia Na-D , 20 ° C | ||||||||||||||||||||||
Ester n- propylowy kwasu (zgodnie z nomenklaturą IUPAC: N-propylo octanu metylu , znany również jako octan n-propylu ) jest organiczno-chemiczny związek z grupy, do estrów kwasów karboksylowych . Wraz ze związkiem izomerycznym octan izopropylu tworzy grupę octanów propylu .
Wydobycie i prezentacja
Przemysłowa produkcja n- propylu przebiega tak daleko, jak to możliwe przez bezpośrednią estryfikację z kwasu octowego, z n- propanolu , w temperaturze 90-120 ° C w silnie kwaśnych żywic kationitowych jako katalizatora .
Reakcję prowadzi się w reaktorze rurowym ze złożem nieruchomym, a utworzoną wodę usuwa się w sposób ciągły z mieszaniny reakcyjnej (przesuwając równowagę na stronę produktu).
W laboratorium lub na mniejszą skalę jako katalizatory stosuje się również mocne kwasy mineralne, takie jak kwas siarkowy lub solny , a często także kwas p- toluenosulfonowy .
nieruchomości
Właściwości fizyczne
Ester n- propylowy kwasu octowego jest bezbarwną cieczą wrzącą w temperaturze 101,5 ° C pod normalnym ciśnieniem . Ciepło parowania w punkcie wrzenia wynosi 33,92 kJ mol -1 . Według Antoine'a funkcja prężności pary wynika z log 10 (P) = A− (B / (T + C)) (P w barach, T w K) przy A = 4,14386, B = 1283,861 i C = -64,378 w zakres temperatur od 312,22 do 374,03 K. Posiada ciepło właściwe przy 25 ° C 196,07 J · K -1 · mol -1 lub 1,92 J · K -1 · g -1 , jeden Napięcie powierzchniowe 24,28 mN / m , standardowa entalpia parowania 39,77 kJ / mol, stała dielektryczna 6,002 i lepkość 0,58 mPa · s (każdorazowo w 20 ° C).
Parametry związane z bezpieczeństwem
Ester n- propylowy kwasu octowego tworzy wysoce łatwopalne mieszaniny par z powietrzem. Związek ma temperaturę zapłonu 10 ° C. Zakres wybuchowości wynosi od 1,7% objętości (70 g / m 3 ) jako dolna granica wybuchowości (DGW) do 8,0% objętości (340 g / m 3 ) jako górna granica wybuchowości (LEU).) Maksymalne ciśnienie wybuchu wynosi 8,6 bara. Wyznaczono graniczną szerokość szczeliny na 1,04 mm. Powoduje to przypisanie do grupy wybuchowości IIA. Temperatura zapłonu wynosi 455 ° C. Dlatego substancja należy do klasy temperaturowej T1.
posługiwać się
Ester n- propylowy kwasu octowego jest stosowany jako rozpuszczalnik w farbach, farbach drukarskich oraz przemyśle chemiczno-technicznym (np. Do kosmetyków i klejów). Posiada dobrą zdolność rozpuszczania wielu żywic naturalnych i syntetycznych (np. Azotanu celulozy ) i jest łatwo biodegradowalny.
Toksykologia / Ocena ryzyka
Opary estru n- propylowego kwasu octowego działają narkotycznie na ludzi.
Ester n- propylowy kwasu octowego został włączony przez UE w 2015 r. Zgodnie z rozporządzeniem (WE) nr 1907/2006 (REACH) w ramach oceny substancji w bieżącym planie działań Wspólnoty ( CoRAP ). Wpływ substancji na zdrowie ludzi i środowisko podlega ponownej ocenie i, jeśli to konieczne, podejmuje się działania następcze. Przyczynami absorpcji octanu n- propylu były obawy dotyczące stosowania przez konsumentów , narażenia pracowników , wysokiego (zagregowanego) tonażu, innych zagrożeń związanych z zagrożeniami i powszechnego stosowania, a także potencjalne ryzyko związane z właściwościami reprodukcyjnymi . Ponowna ocena ma zostać przeprowadzona przez Irlandię od 2021 roku .
linki internetowe
- Wpis dotyczący octanu propylu w Spectral Database for Organie Compounds (SDBS) National Institute of Advanced Industrial Science and Technology (AIST)
Indywidualne dowody
- ↑ wpis do PROPYL ACETATE w bazie CosIng Komisji Europejskiej, dostęp 29 czerwca 2020
- ↑ b c d e f g h i j k l m N O P Q r wejście na octanu propylu w bazie substancji GESTIS o w IFA , do których dostęp 8 stycznia 2020 r. (Wymagany JavaScript)
- ↑ a b BASF: octan n-propylu , dostęp 2 lutego 2020 r
- ^ Wilhelm Riemenschneider, Hermann M. Bolt: Estry, organiczne. W: Encyklopedia chemii przemysłowej Ullmanna . Wiley - VCH Verlag GmbH & Co. KGaA., 30 kwietnia 2005, s. 247, doi : 10.1002 / 14356007.a09_565.pub2 .
- ↑ Wpis na propylu w wykazie klasyfikacji i oznakowania w Europejskiej Agencji Chemikaliów (ECHA), dostępne w dniu 1 lutego 2016 roku producenci lub dystrybutorzy mogą rozwinąć się zharmonizowanej klasyfikacji i oznakowania .
- ↑ Swiss Accident Insurance Fund (Suva): Limit values - aktualne wartości MAK i BAT (szukaj 109-60-4 lub octanu n-propylu ), dostęp 2 listopada 2015 r.
- ↑ a b Patent EP0066059B1 : Proces estryfikacji kwasu octowego alkoholami C2 do C5. Opublikowane 28 listopada 1984 r. , Wnioskodawca: Chemische Werke Hüls AG, wynalazca: Helmut Alfs, Werner Böxkes, Erwin Vangermain.
- ↑ Wpis dotyczący octanu propylu. W: Römpp Online . Georg Thieme Verlag, ostatnia wizyta 21 listopada 2018.
- ↑ Svoboda, V .; Vesely, F .; Holub, R.; Pick, J .: Ciepło odparowania octanów alkilu i propionianów w Collect. Czech. Chem. Commun. 42 (1977) 943-951.
- ↑ a b Majer, V .; Svoboda, V .: Enthalpies of Vaporization of Organic Compounds: A Critical Review and Data Compilation , Blackwell Scientific Publications, Oxford, 1985, 300.
- ↑ Polák, J.; Mertl, I .: Nasycona prężność par octanu metylu, octanu etylu, octanu n-propylu, propionianu metylu i propionianu etylu w kolekcji Collect. Czech. Chem. Commun. 30 (1965) 3526-3528, doi : 10.1135 / cccc19653526 .
- ↑ Jimenez, E.; Romani, L.; Paz Andrade, MI; Roux-Desgranges, G.; Grolier, J.-PE: Molar nadmiar ciepła pojemności i objętości dla mieszanin alkanianów z cykloheksanem w 25 ° C w J. Solution Chem. 15 (1986) 879-890, doi : 10.1007 / BF00646029 .
- ↑ a b c E. Brandes, W. Möller: Parametry związane z bezpieczeństwem. Tom 1: Płyny i gazy łatwopalne. Wirtschaftsverlag NW - Verlag für neue Wissenschaft, Bremerhaven 2003.
- ↑ Wspólnotowy kroczący plan działań ( CoRAP ) Europejskiej Agencji Chemikaliów (ECHA): octan propylu , dostęp 26 marca 2019 r.