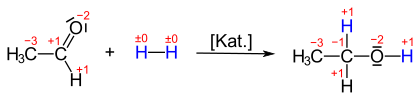Redukcja (chemia)
Redukcja jest reakcja chemiczna, w której jon lub atom jako taki lub jako część cząsteczki przyjmuje jeden lub więcej elektronów , a przez to obniża jego stopień utlenienia . Na obniżenie stopnia utlenienia formalnie wskazuje obniżenie tzw. stopnia utlenienia atomu w cząsteczce odpowiedzialnego za redukcję. Spadek stopnia utlenienia odpowiada liczbie zaabsorbowanych elektronów. Środek redukujący to substancja, atom, jon lub cząsteczka, która oddała elektrony i w ten sposób ulega utlenieniu . Oba połączone reakcje nazywany dwóch częściowych reakcji w reakcji redoks , który ma miejsce
historia
We wczesnych dniach chemii redukcja była postrzegana jako usuwanie tlenu z tlenku . Reakcja, w której utlenianie zostało odwrócone, nazwano redukcją (od łacińskiego reductio oznaczającego „powrót”) . Utlenianie zdefiniowano jako połączenie związku lub pierwiastka z tlenem, co zostało oparte na odkryciach Antoine'a Laurenta de Lavoisiera .
Tlenki metali szlachetnych, takich jak tlenek srebra(I) , rozpadają się po prostu po podgrzaniu. Z tlenku srebra (I) powstaje tlen i srebro pierwiastkowe .
Jeśli tlenek miedzi (II) jest ogrzewany w strumieniu wodoru, powstaje metaliczna miedź i woda . Wodór działa tu jako czynnik redukujący i usuwa tlen z tlenku miedzi (II).
Odpowiednio, tlenek żelaza (III) wytwarza metaliczne żelazo i wodę, a tlen jest usuwany z tlenku żelaza (III).
Obecnie istnieje szerszy pogląd, który nie ogranicza się do reakcji związków zawierających tlen i który integruje pogląd klasyczny.
ogólna definicja
Redukcja to reakcja, w której jedno- lub wieloatomowa cząstka Ox przyjmuje jeden lub więcej elektronów. Powstaje cząstka czerwona:
Ox reaguje jako akceptor elektronów , Ox i Red tworzą tak zwaną parę redoks . Elektrony pochodzą z drugiej pary redoks, która podlega utlenianiu. Podczas gdy w dziedzinie elektrochemii , tak jak w elektrolizie lub ogniwie galwanicznym , przeniesienie elektronu między dwiema parami redoks jest zmienną mierzalną, w innych przypadkach redukcję można rozpoznać tylko po towarzyszącym obniżeniu stopnia utlenienia Ox.
Jeśli redukcja jest postrzegana jako reakcja równowagowa, reakcja odwrotna jest utlenianiem. Taka równowaga istnieje na przykład w nieużywanym akumulatorze . Podczas gdy częściowa reakcja przebiega podczas rozładowywania w jednym kierunku, ładowanie prowadzi do odwrócenia kierunku reakcji.
Chociaż redukcja nigdy nie zachodzi bez utleniania i dlatego zachodzi reakcja redoks, reakcja jest często postrzegana z perspektywy pożądanego produktu. Mówi się o redukcji rudy żelaza do pierwiastkowego żelaza lub katodowej redukcji tlenku glinu do glinu .
Absorpcja elektronów - redukcja stopnia utlenienia
Jeśli żelazny gwóźdź zostanie umieszczony w wodnym roztworze siarczanu miedzi (II) , na paznokciu tworzy się czerwono-brązowa powłoka metalicznej miedzi. Miedź jest redukowana, a żelazo utlenia się do jonów Fe 2+ .
Żelazo, które samo utlenia się podczas reakcji redoks, nazywane jest również w tym kontekście reduktorem , ponieważ jego obecność umożliwia przede wszystkim redukcję miedzi. Redukcja zawsze oznacza zmniejszenie stopnia utlenienia spowodowane wychwytywaniem elektronów. Z kolei utlenianie oznacza uwalnianie elektronów, a tym samym wzrost stopnia utlenienia. W tym przypadku ładunki na cząstkach odpowiadają ich stopniowi utlenienia.
Rozkład termiczny tlenku srebra(I) ze stopniami utlenienia jest również reakcją, w której przenoszone są elektrony.
Gdy tlenek miedzi reaguje z wodorem, miedź ulega redukcji. Wodór działa tu jako środek redukujący. Stan utlenienia atomów tlenu pozostaje niezmieniony w reakcji, ale atomy zmieniają swojego partnera wiążącego. W formalnie utworzone H + jony połączone z formalnie niezmienionej O 2- jonów w celu wytworzenia produktu reakcji wody z utlenienia .
Odpowiednio, żelazo jest redukowane, gdy tlenek żelaza (III) reaguje z wodorem.
Dodatek wodoru
Wychwyt wodoru przez związki organiczne prowadzi do zmniejszenia stopnia utlenienia jednego lub więcej atomów węgla. Katalityczne uwodornienie z 2-buten prowadzi do n- butan :
Stopnie utlenienia atomów węgla wcześniej połączonych wiązaniami podwójnymi zmieniają się od -1 do -2. Formalnie atomy te zajęły jeden elektron i jeden proton . 2. pary redoks ze środkiem redukującym H 2 można wytwarzać w następujący sposób:
W tej reakcji wodór jest formalnie utleniany, a elektrony są formalnie uwalniane. Cała reakcja jest reakcją redoks, z perspektywy eduktu 2-butenu związek redukuje się do n- butanu. Często ta reakcja jest postrzegana jako reakcja addycji . Z tego punktu widzenia zmiany stanów utlenienia nie mają znaczenia.
Redukcja jest często stosowana w połączeniu ze związkami organicznymi zawierającymi tlen, takimi jak konwersja ketonów lub aldehydów w alkohole . Jeśli aldehyd octowy absorbuje wodór, powstaje etanol . Stopień utlenienia grupy karbonylowej zmienia się od +1 do -1:
Redukcje są ważne w biochemii . W wielu szlaków metabolicznych w a komórki , zmniejszenie odbywa się przez przeniesienie wodoru. Koenzymy takie jak NADH , NADPH lub FADH są zdolne do formalnego przeniesienia jonu wodorkowego lub wodoru do innego związku.
Zobacz też
Indywidualne dowody
- ↑ Duden , Niemiecki słownik uniwersalny , wydanie 4, Mannheim, 2001; zobacz także Duden online
- ↑ PONS Online Niemiecki - Łaciński
- ^ Arnold F. Holleman, Nils Wiberg: Podręcznik chemii nieorganicznej , wydanie 102, de Gruyter, Berlin, 2007, s. 218ff.
- ↑ Paula Yurkanis Bruice: Chemia organiczna , Pearson Education, Monachium, wydanie 5, 2011, s. 823ff.
- ↑ Reakcja odwrotna zgodnie z trzecim kryterium definicji utleniania, patrz wpis dotyczący utleniania . W: Kompendium terminologii chemicznej IUPAC („Złota Księga”) . doi : 10.1351 / goldbook.O04362 Wersja: 2.3.1.

![\ mathrm {2 \ Ag_2O \ \ xrightarrow [] {\ Delta} \ 4 \ Ag \ + \ O_2}](https://wikimedia.org/api/rest_v1/media/math/render/svg/92b1a2d90a7393866541de09f446b2b0678982bd)
![\ mathrm {CuO \ + \ H_2 \ \ xrightarrow [] {\ Delta} \ Cu \ + \ H_2O}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f6080949767d7c06542708d1222f2e9f2b46fa78)
![{\ displaystyle \ mathrm {Fe_ {2} O_ {3} \ + \ 3 \ H_ {2} {\ xrightarrow [{}] {\ Delta}} \ 2 \ Fe + \ 3 \ H_ {2} O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/83f8f213748df8aea773d67a4a6834037dadd392)


![\ mathrm {\ \ xrightarrow [] {redukcja}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6cbe51c4c320c6601a67b9a9bcd8d76d527245ba)

![\ mathrm {\ \ xleftarrow [utlenianie] {}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4048ca773f2df6398d9db2dfb0ff737cff823884)