Glukokinaza
| Glukokinaza | ||
|---|---|---|
| ||
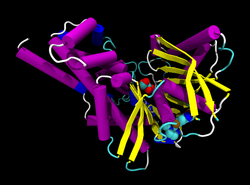
| Model wstążkowy ludzkiej glukokinazy z glukozą i aktywatorem MRK w postaci sferycznych czapek , według PDB 3F9M | ||
| Właściwości białka ludzkiego | ||
| Podstawowa struktura masy / długości | 465 aminokwasów | |
| Izoformy | 3 | |
| Identyfikator | ||
| Nazwa genu | GCK | |
| Identyfikatory zewnętrzne | ||
| Klasyfikacja enzymów | ||
| WE, kategoria | 2.7.1.2 , kinaza | |
| Typ odpowiedzi | Fosforylacja | |
| Podłoże | D -glukoza + ATP | |
| Produkty | D -glukozo-6-fosforan + ADP | |
| Występowanie | ||
| Rodzina homologii | Glukokinaza | |
| Takson macierzysty | Euteleostomi | |
Glukokinaza (GCK) (Hexokinase IV) to nazwa enzymu z grupy heksokinaz, który fosforyluje D- glukozę do glukozo-6-fosforanu u kręgowców (razem z innymi heksozami) .
Istnieją trzy izoformy enzymu u ludzi ; To inicjuje magazynowanie cukru w postaci glikogenu w wątrobie ; W trzustce reakcja reguluje wydzielanie insuliny . Mutacje w GCK genie może prowadzić specjalną formę początku cukrzycy ( MODY 2) i wrodzona hipoglikemii (HHF3).
Inne heksokinazy (które akceptują inne heksozy jako substrat, EC 2.7.1.1 ) są zlokalizowane w mózgu, mięśniach, oczach, nerkach i jelitach.
funkcjonować
Wchodząc w glikolizę , glukoza (Glc) jest fosforylowana przy atomie C6 do glukozo-6-fosforanu (G-6P). Do katalizy tej reakcji służy kilka enzymów, heksokinazy i glukokinaza. Glukokinazę można znaleźć tylko w wątrobie (hepatocytach) i komórkach β trzustki ; w pozostałej części organizmu za fosforylację glukozy odpowiadają heksokinazy.
Heksokinazy
W hexokinases wiązania glukozy o wysokim powinowactwie , co odpowiada K m wartości 0,01 mm i może być zahamowana przez ich końcowego produktu. W erytrocytach pośredni 2,3-difosfoglicerynian, utworzony przez enzym mutazę bisfosfoglicerynianu w cyklu Rapoport-Luebering , będący drogą obejściową do glikolizy, działa również jako inhibitor heksokinaz.
Ze względu na niską wartość Km, heksokinazy działają w zakresie nasycenia w odniesieniu do glukozy zarówno przy stężeniu glukozy we krwi 4 mmol / l w fazie po absorpcji, jak i przy 8-10 mmol / l glukozy w fazie absorpcji. W ten sposób hexokinases miały K m wartości dla glukozy, która jest znacznie niższa niż najniższe stężenie glukozy we krwi. Zapewnia to, że mięśnie, mózg itp. Mogą przemycać glukozę z krwi do glikolizy, jeśli jest to konieczne, niezależnie od sytuacji metabolicznej.
Glukokinaza
Glukokinaza ma mniejsze powinowactwo, jej wartość Km jest w zakresie stężenia glukozy w surowicy, nie może być hamowana przez G-6P i wykazuje (pozytywne) kooperatywne zachowanie wiązania. Ma to kluczowe znaczenie dla ich roli w układzie wykrywania cukru we krwi w trzustce.
Regulacja glukokinazy odbywa się poprzez odwracalne kompleksowanie z białkiem regulującym glukokinazy (GkRP). Wiązanie jest stymulowane przez fruktozo-6-fosforan i sorbitolo-6-fosforan , ale utrudniane przez fruktozo-1-fosforan . Ten ostatni w ten sposób zwiększa aktywność glukokinazy. Po translokacji do jądra kompleks jest rozdzielany, gdy poziom glukozy jest wysoki, a glukokinaza wraca do cytozolu.
porównanie
Poniższy rysunek porównuje krzywe nasycenia glukokinazy i heksokinazy
Rysunek: Krzywe nasycenia glukozy dla heksokinazy (żółta górna hiperbola odpowiadająca Km = 0,01 mM) i hipotetyczna kinaza z Km = 5,5 mM (żółta, płaska dolna hiperbola). Glukokinaza trzustki podąża za punktami pomiarowymi między tymi skrajnościami, ma następujące parametry kooperatywności według Hilla: Km (av) = 5,5 mM (średnia stała Michaelisa); nH = 3 (współczynnik Hilla); Obszar zaznaczony na niebiesko wskazuje zakres wahań stężenia cukru we krwi, tj. H. poziom glukozy we krwi.
Krzywa glukokinazy odpowiednio pokazuje liniowy przebieg w zakresie fizjologicznych stężeń cukru we krwi, tj. H. jeśli poziom Glc rośnie proporcjonalnie, więcej Glc jest przekształcane w G-6P i usuwane z krwiobiegu.
Ostatnio, poprzez systematyczne badanie syntetycznych związków, odkryto aktywator (RO-28-1675) glukokinazy, który działa zarówno na enzymy wątrobowe, jak i trzustkowe. Może to umożliwić nową zasadę leczenia cukrzycy (typu 2).
linki internetowe
Indywidualne dowody
- ↑ Dokumentacja PROSITE PDOC00370. Heksokinazy. Swiss Institute of Bioinformatics (SIB), dostęp 20 września 2011 (angielski).
- ↑ UniProt P35557
- ^ Scott Goodman: metabolizm węglowodanów. W: kumc.edu. University of Kansas, 1999, obejrzano 20 października 2019 .
- ^ Sigurd Lenzen: Świeże spojrzenie na glikolizę i regulację glukokinazy: historia i obecny stan. W: Journal of Biological Chemistry. 289, 2014, s. 12189, doi : 10.1074 / jbc.R114.557314 .
- ↑ Liu F, Dong Q, Myers AM, Fromm HJ: Ekspresja heksokinazy ludzkiego mózgu w Escherichia coli: oczyszczanie i charakterystyka eksprymowanego enzymu . W: Biochem. Biophys. Res. Commun. . 177, nr 1, maj 1991, str. 305-11. PMID 2043117 .
- ↑ Palma F, Agostini D, Mason P, i wsp . : Oczyszczanie i charakterystyka domeny karboksylowej ludzkiej heksokinazy typu III wyrażonej jako białko fuzyjne . W: Mol. Celi. Biochem. . 155, nr 1, luty 1996, str. 23-9. PMID 8717435 .
- ↑ reactome.org: Negatywna regulacja glukokinazy przez białko regulujące glukokinazę




