Chlorek glinu
| Struktura krystaliczna | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
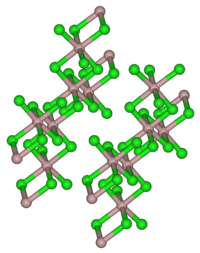
| |||||||||||||||||||
| _Al 3+ _Cl - | |||||||||||||||||||
| System kryształów |
Jednoskośny |
||||||||||||||||||
| Grupa kosmiczna |
C 2 / m (nr 12) |
||||||||||||||||||
| Generał | |||||||||||||||||||
| Nazwisko | Chlorek glinu | ||||||||||||||||||
| inne nazwy |
|
||||||||||||||||||
| Wzór na współczynnik | AlCl 3 | ||||||||||||||||||
| Krótki opis |
ciało stałe o barwie białej do żółtawej o ostrym zapachu |
||||||||||||||||||
| Zewnętrzne identyfikatory / bazy danych | |||||||||||||||||||
| |||||||||||||||||||
| Informacje o narkotykach | |||||||||||||||||||
| Klasa leków | |||||||||||||||||||
| nieruchomości | |||||||||||||||||||
| Masa cząsteczkowa | 133,34 g mol -1 | ||||||||||||||||||
| Stan fizyczny |
mocno |
||||||||||||||||||
| gęstość |
2,44 g cm −3 |
||||||||||||||||||
| Punkt sublimacji |
180 ° C (262 ° C rozkład) |
||||||||||||||||||
| rozpuszczalność |
dobry w wodzie (450 g l −1 w 20 ° C, rozkład) |
||||||||||||||||||
| instrukcje bezpieczeństwa | |||||||||||||||||||
| |||||||||||||||||||
| Dane toksykologiczne | |||||||||||||||||||
| Właściwości termodynamiczne | |||||||||||||||||||
| ΔH f 0 |
−704 kJ mol −1 |
||||||||||||||||||
| O ile to możliwe i zwyczajowe, stosuje się jednostki SI . O ile nie zaznaczono inaczej, podane dane dotyczą warunków standardowych . | |||||||||||||||||||
Chlorek glinu jest nieorganicznym związkiem chemicznym; to jest chlorek z aluminium o wzorze empirycznym AlCl 3 .
synteza
Wodny chlorek glinu ( heksahydrat AlCl 3 · 6H 2 O występujący w kryształach rombowych ) powstaje przez rozpuszczenie glinu w kwasie solnym :
Jednak tego heksahydratu nie można odwodnić, ponieważ po podgrzaniu rozkłada się na wodorotlenek glinu lub metawodorotlenek glinu i gazowy chlorowodór :
Bezwodny chlorek glinu musi być wytwarzany przez przepuszczenie chloru nad węglem i tlenkiem glinu w temperaturze około 800 ° C lub bezpośrednio z pierwiastków:
odpowiednio:
Do produkcji chlorku glinu na dużą skalę stosuje się emaliowane zbiorniki z mieszadłem ze względu na wysoki poziom agresywności stosowanych reagentów.
nieruchomości
Chlorek glinu tworzy bezbarwne, heksagonalne kryształy ( jednoskośna struktura krystaliczna, grupa przestrzenna C 2 / m (grupa przestrzenna nr 12) , a = 5,914 A , b = 10,234 A, c = 6,148 A, β = 108,25 °). Jest rozpuszczalny w wielu rozpuszczalnikach organicznych . Proszek, który jest przeważnie jasnożółty z powodu zanieczyszczenia chlorkami żelaza, ma działanie bardzo higroskopijne . W wilgotnym powietrzu pali się z powodu częściowej hydrolizy do chlorowodoru i tlenochlorku glinu. Rozpuszcza się w wodzie podczas intensywnego ogrzewania, tworząc heksahydrat . W rozpuszczalnikach niepolarnych , w fazie ciekłej i w stanie pary, chlorek glinu występuje jako dimer (Al 2 Cl 6 ), w którym atom glinu jest koordynowany tetraedrycznie (analogicznie do bromku glinu ). W stanie stałym istnieje sieć jonowa, w której jon glinu jest koordynowany 6-krotnie przez Cl - . Podczas topienia sieć jonowa rozpada się, tworząc dimer. Ponieważ ma strukturę kowalencyjną, ciekły chlorek glinu słabo przewodzi prąd.
Związki wiązania w chlorku glinu (III) są klasyfikowane jako przypadek graniczny między wiązaniem kowalencyjnym i jonowym , ma on różnicę elektroujemności ΔEN 1,55 (według Paulinga). Więc właściwie powinno to być polarne wiązanie atomowe .
Reakcja na coś
W reakcji silnie egzotermicznej chlorek glinu rozpuszcza się w wodzie , z hydrolizą w jonach chlorkowych i kompleksach glinu hexaaqua :
Te jony glinu hexaaqua działają jak słaby kwas (p K s = 4,97):
Hydrat nie może być odwodniony przez ogrzewanie do bezwodnego chlorku glinu, ponieważ uwolnienie wody i chlorowodoru powoduje powstanie wodorotlenku glinu lub tlenku glinu.
posługiwać się
Sześciowodzian chlorku glinu ze względu na swoje silne działanie ściągające znajduje zastosowanie w przemyśle tekstylnym i mydlniczym, gdzie jest wykorzystywany m.in. do produkcji środków antyseptycznych czy dezodorantów . Działa także jako silny kwas Lewisa i organicznego syntezy (głównie bezwodny tutaj) jako katalizatora w odwodornienia , polimeryzacji i reakcji Friedel-Craftsa ( Friedela-Craftsa , Friedla-Craftsa ). Jest również stosowany jako nośnik halogenowy i środek kondensujący.
W przypadku lekkiego zapalenia gardła do płukania gardła proponuje się roztwory zawierające chlorek glinu lub chloran glinu . Jest dostępny bez recepty w aptekach i drogeriach.
Chlorek glinu jest stosowany w chromatografii cienkowarstwowej w postaci odczynnika w sprayu do wykrywania flawonoidów . W tym celu 2,0 g heksahydratu chlorku glinu rozpuszcza się w 100 ml 5% roztworu (V / V) lodowatego kwasu octowego w metanolu . Po rozpyleniu tego roztworu na płytkę TLC, ogląda się go w świetle UV 365 . Odczynnik ten jest wymieniony pod nazwą odczynnik chlorku glinu R w Farmakopei Europejskiej (Ph. Eur.).
instrukcje bezpieczeństwa
W 2014 r. Chlorek glinu został uwzględniony w bieżącym planie działań UE ( CoRAP ) zgodnie z rozporządzeniem (WE) nr 1907/2006 (REACH) w ramach oceny substancji . Wpływ substancji na zdrowie ludzi i środowisko podlega ponownej ocenie i, w razie potrzeby, podejmuje się działania następcze. Przyczyną absorpcji chlorku glinu były obawy o narażenie pracowników , wysoki (zagregowany) tonaż i wysoki współczynnik charakterystyki ryzyka (RCR), a także zagrożenia wynikające z ewentualnego przypisania do grupy substancji CMR . Ponowna ocena trwa od 2015 r. I jest prowadzona przez Francję . Aby móc dokonać ostatecznej oceny, zażądano dalszych informacji.
Przygotowania handlowe
AHC20 (CH), AHC30 (CH), Everdry (D), Gargarisma zum Gurgeln (D), Mallebrin (D), Never-Sweat (D), Odaban (GB), Seven days (D), Sweat Protect (D) , Yerka (D), Purax (D)
Zobacz też
Indywidualne dowody
- ↑ Wpis dotyczący CHLORKU ALUMINIUM w bazie danych CosIng Komisji Europejskiej, dostęp 28 grudnia 2020 r.
- ↑ Wprowadzenie na temat chlorku glinu. W: Römpp Online . Georg Thieme Verlag, ostatnia wizyta 11 listopada 2014.
- ↑ a b c d e f arkusz danych chlorku glinu (PDF) firmy Merck , dostęp 4 lutego 2017 r.
- ↑ Wpis na chlorek glinu w bazie substancji GESTIS z tej IFA , dostępne w dniu 10 stycznia 2017 roku. (Wymagany JavaScript)
- ↑ Wpis na chlorek glinu w wykazie klasyfikacji i oznakowania w Europejskiej Agencji Chemikaliów (ECHA), dostępne w dniu 1 lutego 2016 roku producenci lub dystrybutorzy mogą rozwinąć się zharmonizowanej klasyfikacji i oznakowania .
- ↑ Kolekcja receptur PAETEC wydanie 2003, s.116.
- ↑ SI Troyanov: Struktury krystaliczne tetrachloroglinianów tytanu Ti (AlCl 4 ) 2 i udoskonalenie kryształu struktury AlCl 3 . W: Russian Journal of Inorganic Chemistry. 37, 1992, str. 266-272.
- ^ NN Greenwood, A. Earnshaw: Chemia pierwiastków Wiley-VCH, 1990, ISBN 3-527-26169-9 .
- ^ AF Hollemann, N. Wiberg: Podręcznik chemii nieorganicznej . Wydanie 102. De Gruyter, Berlin 2007, ISBN 978-3-11-017770-1 , s. 1158 .
- ↑ G. Jander, E. Blasius: Podręcznik analitycznej i preparatywnej chemii nieorganicznej. Edycja 12. S. Hirzel Verlag, Leipzig 1982, s. 275.
- ^ AF Hollemann, N. Wiberg: Podręcznik chemii nieorganicznej . Wydanie 102. De Gruyter, Berlin 2007, ISBN 978-3-11-017770-1 , s. 1152 .
- ↑ E. Merck AG (Ed.): Odczynniki barwiące do chromatografii cienkowarstwowej i bibułowej . Darmstadt 1965, s. 1 .
- ↑ Farmakopea Europejska . Wydanie 4.00. taśma 1 . Deutscher Apotheker Verlag / Govi-Verlag - Pharmazeutischer Verlag GmbH, Stuttgart / Eschborn 2002, ISBN 3-7692-2947-9 , s. 375 .
- ↑ Wspólnotowy kroczący plan działań ( CoRAP ) Europejskiej Agencji Chemikaliów (ECHA): Chlorek glinu , dostęp 26 marca 2019 r.








![{\ Displaystyle {\ ce {AlCl3 + 6H2O -> [Al (H2O) 6] ^ {3 +} {} + 3Cl-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7fa18725451127cd374cc0e67c39c572d35f1c95)
![{\ Displaystyle {\ ce {[Al (H2O) 6] ^ {3 +} {} + H2O -> [Al (H_ {2} O) _ {5} OH] ^ {2 +} {} + H3O + }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5d462c22a0409097f3104c2dea610676039b789b)
![{\ Displaystyle {\ ce {[Al (H2O) 6] Cl3 -> Al (OH) 3 + 3HCl + 3H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a16f12d8111c10611ecd33c5381c22618a8b5fb9)
![{\ Displaystyle {\ ce {2 [Al (H2O) 6] Cl3 -> Al2O3 + 6HCl + 9H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/73ec7c6511903fd86ee2ba49910a19cb289adbb6)
