Węglowodory
| Węglowodory |
 metan |
 Etan |
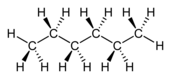 n -heksan |
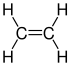 Ethene |
 Propen |
|
Etyka |
 benzen |

Do węglowodorów są grupy związków chemicznych , które składają się wyłącznie z węgla i wodoru . Ta grupa substancji jest zróżnicowana, ponieważ węglowodory mogą zawierać łańcuchy , pierścienie węglowe lub ich kombinacje. Istnieje kilka podgrup, takich jak alkany , alkeny , alkiny i związki aromatyczne (areny). Węglowodory zyskały duże znaczenie techniczne przede wszystkim dzięki ich wykorzystaniu jako paliw kopalnych oraz w syntezie organicznej .
Występowanie
W naturze węglowodory występują w bardzo dużych ilościach, zwłaszcza w ropie naftowej i gazie ziemnym , dlatego te dwa zasoby mineralne są również podsumowane pod wspólnym terminem węglowodory kopalne . Występują również w wielu roślinach np. B. jako terpeny , karotenoidy i kauczuk , a więc są skamieniałe w węglu . Proste węglowodory, zwłaszcza metan , są produktami metabolizmu niektórych mikroorganizmów. W kosmosie węglowodory, głównie w postaci metanu i etanu , znaleziono na kometach, planetach i księżycach, a także w materii międzygwiazdowej.
Systematyka
Węglowodory można podzielić na aromatyczne i alifatyczne , w których wyróżnia się związki nienasycone i nasycone .
W węglowodorach nasyconych występują związki chemiczne, które zawierają wyłącznie pojedyncze wiązania C-C . Są podzielone na połączenia w kształcie łańcuchów i pierścieni. Formy łańcuchowe są systematycznie nazywane alkanami . Najprostszymi i najbardziej znanymi alkanami są metan (CH 4 ), etan (C 2 H 6 ) i propan (C 3 H 8 ). Ogólnie rzecz biorąc, empiryczny wzór na homologiczną serię łańcuchowych alkanów to C n H 2n + 2 . Alkany w kształcie pierścienia nazywane są cykloalkanami . Ich ogólny wzór empiryczny na szereg homologiczny to C n H 2n .
Węglowodory nienasycone można podzielić na alkeny i alkiny . Alkeny to związki zawierające podwójne wiązania C = C. Najprostszym przedstawicielem tej grupy substancji jest eten , zwany także etylenem (C 2 H 4 ). Najprostsze n- alkeny z tylko jednym wiązaniem podwójnym na ogół mają wzór empiryczny C n H 2n . Związki zawierające co najmniej dwa wiązania podwójne C = C, takich jak 1,3-butadien , określane są jako polieny . Cykloalkeny to cykliczne węglowodory, takie jak cyklopentadien . Tutaj są podwójne wiązania CC w pierścieniu węglowym. Alkiny to węglowodory zawierające jedno lub więcej potrójnych wiązań CC . Najbardziej znanym przedstawicielem jest etyna (acetylen) o wzorze empirycznym C 2 H 2 . Odpowiednio, alkiny z potrójnym wiązaniem generalnie mają wzór empiryczny do homologicznej serii C n H 2n-2 . Węglowodory nasycone i nienasycone zbierane są pod nazwą węglowodory alifatyczne , zwłaszcza w przemyśle petrochemicznym .
Trzecią ważną grupą węglowodorów są węglowodory aromatyczne . Są to węglowodory aromatyczne i zwykle mają pierścienie C 6 (areny). Najbardziej znanym przedstawicielem jest benzen (C 6 H 6 ). Wielopierścieniowe węglowodory aromatyczne stanowią podgrupę aromatów . Są to związki składające się z kilku połączonych ze sobą pierścieni benzenowych. Dobrze znanym przedstawicielem jest naftalen (C 10 H 8 ).
Węglowodory, które w strukturze odpowiadają ciałom stałym platońskim , nazywane są węglowodorami platońskimi . Należą do nich czworościan , kuban i dwunastościan .
Węglowodory o tym samym wzorze empirycznym mogą mieć różne wzory strukturalne (wiązania atomów węgla). Są więc izomerami konstytucyjnymi . Występują w alkanach z butanów i większości innych węglowodorów. Klasyczna izomeria cis - trans czasami występuje na wiązaniach podwójnych CC. Proste rozgałęzione węglowodory mogą, jak pokazuje przykład 3-metyloheksan , być chiralne . Atom węgla w pozycji numer 3 staje się stereocentrum , połączenie jest asymetryczne i rozróżnia się enancjomery ( R ) - i ( S ).
cechy
Wiele węglowodorów niepolarnych jest nierozpuszczalnych w wodzie, ale są one łatwo rozpuszczalne w większości rozpuszczalników organicznych . Oznacza to, że węglowodory są hydrofobowe , czyli także lipofilowe .
Węglowodory gazowe spalają się bardzo szybko iz gorącym płomieniem; uwolniona energia jest wielka. Ciekłe węglowodory o niskiej temperaturze wrzenia łatwo odparowują; Pożary są łatwe do rozpalenia ze względu na ich niską temperaturę zapłonu . Optymalne (całkowite) spalanie węglowodorów wytwarza wodę i dwutlenek węgla , a niewystarczające (niepełne) spalanie może również powodować powstawanie tlenku węgla lub węgla (sadzy). Reaktywność alkanów zależy od długości ich łańcuchów. Alkany o długim łańcuchu są stosunkowo obojętne (mało reaktywne). Jeśli węglowodory palą się przy spalaniu sadzy, może to również oznaczać wyższą zawartość węgla w mieszance (dłuższa długość łańcucha).
Oprócz reakcji redoks, gdy są spalane, alkany wchodzą w reakcje substytucji , w których atomy wodoru mogą być wymieniane na inne atomy i grupy atomów, ale głównie halogeny. Z drugiej strony alkeny i alkiny są bardzo reaktywne i reagują z wieloma substancjami, dodając do wiązania wielokrotnego CC ( reakcja addycji ).
Stosunkowo dużą skłonność atomów węgla w celu wytworzenia łańcuchów CCC- ... (konkatenacji lub katenization, angielski wiązanie , od łacińskiego catena , łańcuch „), ma decydujące znaczenie dla różnych węglowodorów i jest oparty na wyżej energii wiązania w kowalencyjne C - wiązań C (356 kJ / mol) w porównaniu z wyższymi homologami 14. grupy (np.Si - Si (226 kJ / mol), Ge - Ge (186 kJ / mol)). Ponadto wiązanie C - H jest również bardziej stabilne termodynamicznie niż wiązanie Si - H, Ge - H lub Sn - H. To wyjaśnia, dlaczego istnieje większa różnorodność węglowodorów niż węglowodory krzemu lub germanu.
posługiwać się

Alkany są często wykorzystywane jako paliwa kopalne w mieszaninach takich jak biogaz , gaz płynny , benzyna , olej napędowy , olej opałowy , nafta i ropa naftowa . Najważniejszymi alkanami są alkany o niskiej masie cząsteczkowej: metan , etan i propan . Alkany, takie jak n- butan , izopentan , różne heksany i cykloalkan cykloheksan są składnikami benzyny silnikowej .
Węglowodory służą jako materiały wyjściowe w wielu ważnych dla przemysłu procesach syntezy chemicznej. Alkeny, takie jak eten i cykloheksen , alkiny, takie jak acetylen i polieny , takie jak 1,3-butadien , izopren i cyklopentadien mają znaczenie przemysłowe . Wiele arenów ma znaczenie przemysłowe, w tym benzen , toluen , ksylen i styren .
Ważne są produkty polimeryzacji węglowodorów, takich jak polistyren , polietylen , polipropylen , polietylen , wiele kopolimerów i chlorowcowanych polimerów węglowodorowych, takich jak polichlorek winylu i politetrafluoroetylen . Ponadto węglowodory służą jako rozpuszczalniki lipofilowe.
Szkody ekologiczne
Węglowodory stanowią - zgodnie z definicją Światowej Organizacji Zdrowia WHO - główną część lotnych związków organicznych (w skrócie LZO); kiedy są emitowane, uważa się je za szkodliwe dla środowiska. Aby zmniejszyć emisje, z. B. w Szwajcarii nałożył podatek motywacyjny na te emisje . Następnie metan ma znaczący efekt cieplarniany .
Zobacz też
literatura
- Handbook of Experimental Chemistry Secondary Area II, Volume 9, Hydrocarbon, Aulis Verlag Deubner & Co. KG.
- Karl-Heinz Lautenschläger, Werner Schröter, Joachim Teschner, Hildegard Bibrack, Taschenbuch der Chemie , 18. wydanie, Harri Deutsch, Frankfurt (Main), 2001.
- JC Jones: Węglowodory. Właściwości fizyczne i ich znaczenie w użytkowaniu . JC Jones & Ventus Publishing ApS, 2010. ISBN 978-87-7681-513-4 ( PDF w bookboon.com ).
- Hartung, Birgitta (1984) Potencjalne skały macierzyste węglowodorów w głębinach morskich. Nauki o Ziemi w naszych czasach; 2, 6; 208-211; doi : 10.2312 / geosciences.184.2.208 .
linki internetowe
Indywidualne dowody
- ↑ Wejście na temat węglowodorów . W: IUPAC Compendium of Chemical Terminology („Złota Księga”) . doi : 10.1351 / goldbook.H02889 Wersja: 2.3.2.
- ↑ Catherine E. Housecroft, Alan G. Sharpe: Inorganic Chemistry , 4. wydanie, Pearson Education, Amsterdam, 2012, str. 433 i nast.
- ↑ SAEFL : Zanieczyszczenie powietrza w kantonach ., 1997

