Barwniki
Barwniki to barwniki, które w przeciwieństwie do pigmentów są rozpuszczalne w mediach aplikacyjnych, takich jak woda lub inne rozpuszczalniki . Można je klasyfikować według różnych kryteriów, na przykład według ich pochodzenia ( barwniki naturalne / syntetyczne ), zastosowania ( podłoże ), budowy chemicznej ( chromofor ) lub zakresu zastosowania.
Niektóre barwniki można przekształcić w nierozpuszczalne pigmenty przez dodanie środków strącających , patrz lakowanie .
historia
Niewiele wiadomo na temat stosowania barwników w starożytności , ponieważ stosunkowo łatwo ulegają one rozkładowi pod wpływem światła, powietrza i mikroorganizmów . Stosując nowoczesne metody analityczne (np. HPLC ) można jednak wykryć najmniejsze ślady barwników. Niebieską, rozpuszczalną w wodzie indygotynę można było wykryć na tkaninach egipskich, które mają ponad 3000 lat . Uprawa rośliny indygo ( Indigofera tinctoria ) trwa już 2500 lat p.n.e. W Egipcie istnieją na to dowody, a zapisy o procesie barwienia indygo pochodzą z czasów starożytnych ( Papyrus Leidensis , Papyrus Holmiensis). W Europie barwnik ten pozyskiwano z urzetu . Takie podejście stało się nieopłacalne w XVII wieku, kiedy duże ilości indygo sprowadzano z Indii Wschodnich .

Stosowanie prawdziwej purpury , pozyskiwanej z fioletowego ślimaka występującego u wybrzeży wschodniej części Morza Śródziemnego , można udowodnić również w starożytności. W przypadku barwienia na czerwono bardzo kosztowny fiolet został częściowo zastąpiony barwnikiem alizaryną zawartym w marzannie ( Rubia tinctorum ), barwnikiem znanym już przed narodzinami Chrystusa. Inne barwniki pochodzenia naturalnego stosowane od czasów starożytnych to henna , kermes , kurkuma i szafran .
Wraz z "odkryciem" w Ameryce naturalnych barwników do drewna (m.in. Logwood , Redwood , Yellow Wood ) do barwienia tekstyliów i skór, także do farbowania włosów i papieru. Stosowanie prawdziwego karminu , pozyskiwanego z mączlików koszenilowych ( Dactylopius coccus Costa), stało się również popularne w Europie .
Podstawę rozwoju syntetycznych barwników organicznych położono w pierwszej połowie XIX wieku. Friedlieb Ferdinand Runge izolowane i scharakteryzowano w 1834 od smoły , która ubocznym produktem koksu z węgla , w tym aniliny i fenolu . Pierwszy syntetyczny barwnik został odkryty przypadkowo w 1832 roku przez niemieckiego chemika Karla von Reichenbacha i nazwany Pittakall . Chemik August Wilhelm von Hofmann zajmował się od 1843 r. chemią smoły węglowej i opracował wiele nowych wdrożeń i procesów. Uczeń Hofmanna, William Henry Perkin, znalazł w 1856 roku w testach utleniania anilinę Mauvein . Był to pierwszy syntetyczny barwnik wyprodukowany komercyjnie. W kolejnych latach chemia farb smołowych , szczególnie za sprawą prac Hofmanna i jego uczniów Perkina, Johanna Petera Grießa , Carla Alexandra von Martiusa (założyciela Agfy ) i Georga Mercka (założyciela Merck & Co. w Nowym Jorku ), wziął burzliwy rozwój:
- 1856: Pierwsza synteza barwnika trifenylometanu fuksyny przez polskiego chemika Jakuba Natansona
- 1858: Opracowanie i opatentowanie produkcji fuksyny przez francuskiego chemika François-Emmanuela Verguina . Niemal w tym samym czasie August Wilhelm Hofmann opracował alternatywną syntezę fuksyny.
- 1861: Wynalezienie fioletu krystalicznego przez Charlesa Lautha - barwnika z grupy barwników kationowych , który nadaje się do drukowania tuszami , tuszami i papierem bezkalkowym .
- 1862: Rozwój reakcji diazowania jako ważnego etapu pośredniego w syntezie barwników azowych przez Johanna Petera Grießa. Barwniki azowe rozwinęły się w najważniejszą i największą grupę barwników syntetycznych.
- 1863: Wynalezienie brązu Bismarcka przez Martiusa – pierwszego produkowanego komercyjnie barwnika azowego.
- 1869: Pierwsza synteza naturalnego barwnika - alizaryny - przez chemika BASF Heinricha Caro we współpracy z Carlem Graebe i Carlem Liebermannem .
- 1871: Opracowanie syntezy wskaźnika pH fenoloftaleiny z bezwodnika ftalowego i rezorcynolu przez Adolfa von Baeyera .
- 1877: Synteza zieleni malachitowej autorstwa Otto Fischera .
- 1878: Pierwsza pełna synteza indygo Adolfa von Baeyera. Alternatywny proces produkcyjny został opracowany przez Karla Heumanna w 1890 roku , który po dalszych udoskonaleniach doprowadził do przemysłowej produkcji barwnika od 1897 roku. Opłacalna przemysłowa produkcja indygo, która została osiągnięta dzięki dalszej optymalizacji procesu - w szczególności przez chemika Johannesa Pflegera - doprowadziła w ciągu kilku lat do drastycznego zmniejszenia udziału w rynku naturalnie pozyskiwanego indygo.
Pomyślna produkcja i sprzedaż na dużą skalę nowych barwników syntetycznych była ważna dla tego rozwoju. Perkin zabezpieczył swój wynalazek patentem i założył fabrykę chemiczną, w której już w 1857 r . produkowano fioletoworóżowy barwnik do barwienia jedwabiu i bawełny . W Niemczech późniejszy Hoechst AG (2 stycznia 1863 jako Theerfarbenfabrik Meister, Lucius & Co. ) i Bayer AG (1 sierpnia 1863 jako Friedr. Bayer et comp. ) oraz dwa lata później BASF (6 kwietnia) 1865 jako fabryka aniliny i sody w Baden ).
Dalszym rozwojem chemii barwników w XX wieku było wprowadzenie odpornych na światło barwników kadziowych na bazie antrachinonu . Pierwszym przedstawicielem w 1901 roku był barwnik indanthrene blue opracowany przez BASF , z którego rozwinęła się szeroka gama indanthrene. W latach dwudziestych wynalezienie barwników dyspersyjnych umożliwiło barwienie hydrofobowych włókien syntetycznych , takich jak jedwab octanowy czy później włókna poliestrowe . Wraz z rozwojem ftalocyjaniny , zwłaszcza ftalocyjaniny miedzi , w 1935 roku ICI wyprodukowała nowy chromofor zawierający metal, który początkowo był używany jako pigment. Dzięki wprowadzeniu solubilizujących grup kwasu sulfonowego ten chromofor może być również stosowany jako barwnik. W 1951 roku wprowadzono pierwsze reaktywne barwniki do barwienia wełny , a od 1956 reaktywne barwniki do barwienia bawełny. W następnych dziesięcioleciach rozwój barwników tekstylnych skupił się na poprawie właściwości aplikacyjnych. Na przykład poprzez opracowanie dwufunkcyjnych barwników reaktywnych lub barwników reaktywnych z nowymi grupami reaktywnymi.
Oprócz zastosowań tekstylnych na przestrzeni lat coraz częściej skupiano się na barwnikach funkcjonalnych. Termin ten został ukuty w 1993 roku dla barwników, których specyficzne zastosowanie nie opiera się na ich estetycznych właściwościach kolorystycznych. Barwniki funkcjonalne wykorzystywane są m.in. w medycynie, farmacji, fotowoltaice, do przechowywania danych oraz w poligrafii.
Podstawy chemiczno-fizyczne
Widmo światła jest widoczne dla ludzi w zakresie długości fal od 380 do 790 nm. Kiedy białe światło pada na ciało, jego widmo jest częściowo odbijane, a częściowo pochłaniane. Jeżeli np. zaabsorbowane zostaną krótkofalowe składowe barwy światła (od fioletu do błękitu , 420-480 nm), emitowane promieniowanie zawiera głównie składowe długofalowe (do 780 nm) i wrażenie barwy, tzw. kolor ciała , od żółtego do czerwonego .
Barwniki również pochłaniają i odbijają część widzialnego światła białego, a mieszanina barw dopełniających się w pochłanianym świetle jest postrzegana przez oko.

Właściwości barwiące związku chemicznego wynikają z jego budowy chemicznej. Podczas gdy cząsteczki z wiązaniami σ absorbują energię elektromagnetyczną w zakresie promieniowania rentgenowskiego i UV , cząsteczki z elektronami w wiązaniach π (wiązania nienasycone) są już wzbudzane promieniowaniem elektromagnetycznym o mniejszej energii. Jeśli w cząsteczce występuje kilka sprzężonych wiązań nienasyconych, elektrony π ulegają delokalizacji i wraz ze wzrostem stopnia sprzężenia zmniejsza się odległość energetyczna między stanem podstawowym a wzbudzonym stanem energetycznym cząsteczki. Maksimum absorpcji przesuwa się w kierunku dłuższych fal i widzialnego zakresu widma. (→ efekt batochromowy )
Takie struktury molekularne są zgodne z teorią barwników Otto Nikolausa Witta jako odpowiednio chromofory . Grupy funkcyjne w cząsteczce, które działają jako donory elektronów lub jako akceptory elektronów, wpływają na mezomerię w cząsteczce poprzez zwiększanie lub zmniejszanie gęstości elektronowej grupy chromoforowej. Znane są również jako auksochromy lub antyauksochromy.
Grupami auksochromowymi są, na przykład, grupy hydroksylowe , eterowe , aminowe i amidowe , a grupami antyauksochromowymi są grupy karbonylowe , nitrowe , karboksylowe i sulfo .
Klasyfikacja barwników
Najpopularniejsza klasyfikacja różnych barwników opiera się na ich strukturze chemicznej lub na technicznym procesie aplikacji barwienia.
Klasyfikacja według struktur chemicznych
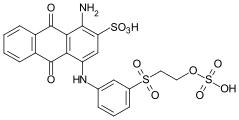
Barwniki antrachinonowe
Podstawową strukturą tej grupy barwników jest antrachinon . Zmieniając podstawniki można uzyskać prawie wszystkie odcienie od żółtego do czerwonego i od niebieskiego do zielonego, przy czym szczególne znaczenie mają czerwony i niebieski barwnik antrachinonowy. Układ chinoidowy można przekształcić w odpowiedni rozpuszczalny w wodzie hydrochinon przez redukcję , tak że barwniki antrachinonowe można stosować jako barwniki kadziowe . Z odpowiednimi podstawnikami barwniki antrachinonowe można stosować jako barwniki dyspersyjne do barwienia włókien syntetycznych. Jako barwniki kwasowe lub reaktywne stosuje się rozpuszczalne w wodzie barwniki antrachinonowe z grupami kwasu sulfonowego .
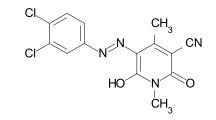
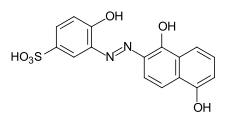
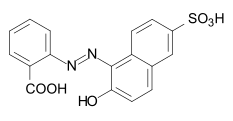
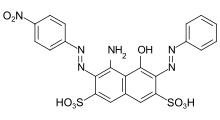
Barwniki azowe
Barwniki azowe zawierają jako podstawową strukturę grupę azową podstawioną przez rodniki arylowe lub alkenylowe . Barwniki azowe z kilkoma grupami azowymi określane są jako barwniki bisazo (również disazo), trisazo, tetrakisazo, polyazo. Podstawnikami arylowymi są zwykle pochodne benzenu lub naftalenu , ale także heterocykliczne związki aromatyczne, takie jak pirazole lub pirydony . Enolizable grup alifatycznych, na przykład podstawione anilidy z kwasu acetylooctowego są stosowane jako alkenyl .
Synteza barwnika odbywa się przez dwuazowanie aminy aromatyczne oraz późniejsze azowych sprzęgających z soli diazoniowej do bogatych w elektrony aromatycznych lub związków β-dikarbonylowych. Barwniki azowe są zdecydowanie najważniejszą i najszerszą grupą barwników i są reprezentowane w prawie wszystkich kategoriach barwników technicznych (→ klasyfikacja według procesów technicznych ). Nie są znane naturalnie występujące barwniki azowe. Z wyjątkiem turkusu lub jaskrawej zieleni , prawie wszystkie odcienie kolorów można uzyskać za pomocą barwników azowych. Grupa azowa jest wrażliwa na czynniki redukujące – ulega rozszczepieniu, w wyniku czego barwnik odbarwia się.
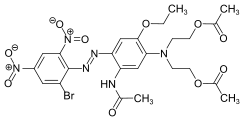
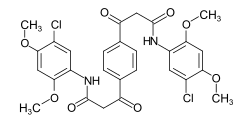
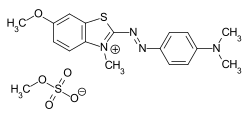
Kilka przykładów różnych typów barwników azowych (barwniki mono i bisazo / benzen, reszty naftalenowe / pirydon, składnik sprzęgający acetoacetanilid / barwnik kompleksowy metalu):
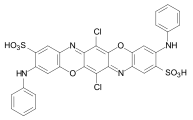
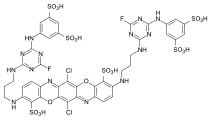
Barwniki dioksazynowe
Barwniki dioksazynowe - znane również jako barwniki trifendioksazynowe - zawierają trifendioksazynę jako podstawową strukturę. Silne, błyszczące barwniki mają dobrą trwałość, dzięki czemu łączą zalety barwników azowych i antrachinonowych. Barwniki dioksazynowe są dostępne w handlu jako barwniki bezpośrednie i reaktywne.
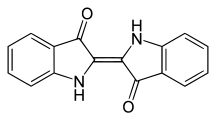
Barwniki indygoidowe
Barwniki indigoidalne należą do barwników karbonylowych i są stosowane jako barwniki kadziowe. Najważniejszym przedstawicielem jest indygo, które pozyskiwano jako naturalny barwnik z roślin w starożytności i które nadal jest produkowane przemysłowo w dużych ilościach i używane w szczególności do barwienia niebieskiego dżinsu .
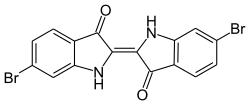
Innym naturalnym barwnikiem jest pradawna purpura ( CI Natural Violet 1 / Dibromoindigo ).
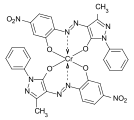
Barwniki metalokompleksowe
Metalokompleksowych barwników są związki koordynacyjne z jonem metalu z jednym lub więcej barwnika ligandów , które donorem elektronów grupy. Dominują związki miedzi i chromu , ale w mniejszym stopniu jako barwniki stosuje się również kompleksy kobaltu , niklu i żelaza . Ligandy często są barwniki azowe , azometinowe barwniki , formazanów lub ftalocyjaniny . Barwniki metalokompleksowe charakteryzują się bardzo dobrą trwałością.
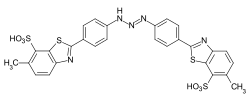
Barwniki formazańskie
Barwniki formazanowe są strukturalnie spokrewnione z barwnikami azowymi. Podstawowa struktura to 1,3,5‑trifenyloformazan . Tworzą kompleksy chelatowe z metalami przejściowymi, takimi jak miedź , nikiel czy kobalt . W zależności od innych podstawników, nieskompleksowane formazany są koloru pomarańczowego do głębokiej czerwieni, formazany z kompleksami metali purpurowe, niebieskie do zielonego. Syntezę prowadzi się przez sprzęganie z soli diazoniowych w hydrazonów .
Znaczenie handlowe mają niebieskie kompleksy chelatowe miedzi czterokleszczowe różnych formazanów, które są wykorzystywane w szczególności jako barwniki reaktywne do bawełny:
Barwniki ftalocyjaniny
Barwniki ftalocyjaninowe są miedź - albo niklu - Kompleksy metali o podstawowej strukturze ftalocyjaniny . Są one strukturalnie spokrewnione z porfirynami , z którymi mają wspólny element aza[18]annelenowy . Dzięki wprowadzeniu rozpuszczalnych w wodzie podstawników - głównie poprzez sulfochlorowanie - dostępne są barwniki od turkusu do jaskrawej zieleni. Barwniki ftalocyjaninowe charakteryzują się doskonałą światłotrwałością.
Barwniki metinowe
Metina lub polimetyna mają jako układ chromoforowy sprzężone wiązania podwójne, z dwiema grupami końcowymi jako akceptor elektronów A i funkcja donora elektronów D. Grupy końcowe, które w większości przypadków zawierają atomy azotu lub tlenu, mogą być częścią heterocyklu, a wiązania podwójne częścią układu aromatycznego. Jeśli jedna lub więcej grup metinowych jest zastąpionych przez atomy azotu, mówi się o aza-analogicznych barwnikach metinowych. Daje to różne podklasy:
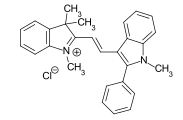
- Barwniki cyjaninowe, w których sprzężone wiązania podwójne są flankowane trzeciorzędową grupą aminową i czwartorzędową grupą amonową . Jeśli dwie grupy metinowe zostaną zastąpione atomami azotu, a jedna grupa końcowa jest częścią heterocyklu, podczas gdy druga grupa końcowa ma łańcuch otwarty, uzyskuje się ważne barwniki diazahemycyjaniny. Przykład: CI podstawowy czerwony 22 .
- Barwniki styrylowe : poprzez wprowadzenie pierścienia fenylowego w strukturę polienową, posiadają styrenowy element strukturalny. Przykład: CI rozproszony żółty 31 .
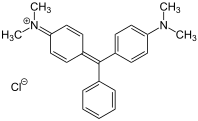
- Barwniki triarylometynowe, określane również w starszej literaturze jako barwniki triarylometanowe , ponieważ pochodzą od trifenylometanu, w którym co najmniej dwa pierścienie aromatyczne mają podstawniki elektronodonorowe. Przykład: CI Basic Green 4 (malachitowa zieleń).
Barwniki nitro i nitrozo
W przypadku barwników nitro, na pierścieniu aromatycznym w pozycji orto względem donora elektronów znajduje się grupa nitrowa - albo grupa hydroksy (-OH) albo grupa aminowa (-NH 2 ). Najstarszym przedstawicielem tej klasy barwników jest kwas pikrynowy (2,4,6-trinitrofenol). Jednak barwniki hydroksynitrowe nie mają już znaczenia handlowego. Jest to stosunkowo niewielka, ale stara klasa barwników, których przedstawiciele charakteryzują się wysoką światłotrwałością i łatwością wykonania. Barwniki nitro mają kolor od żółtego do brązowego. Ponieważ są to stosunkowo małe cząsteczki, ważnym obszarem zastosowania jako barwników dyspersyjnych jest barwienie włókien poliestrowych. Stosowane są również jako barwniki kwasowe i pigmentowe.
Rzadkie barwniki nitrozowe to związki aromatyczne z grupą nitrozową . Barwniki nitrozo z grupą hydroksylową w pozycji orto do grupy nitrozowej są stosowane wyłącznie jako kompleksy metali. Typowym przedstawicielem jest zieleń naftolowa B (CI Acid Green 1).
Barwniki siarkowe
Barwniki siarkowe (barwniki siarczkowe) to nierozpuszczalne w wodzie, wielkocząsteczkowe barwniki, które mają wiązania disiarczkowe lub oligosiarczkowe między rodnikami aromatycznymi. Otrzymuje się je przez stopienie benzenu , naftalenu lub antracen pochodne z siarki lub sodu polisiarczków i mają nierównomierną konstytucji . Nadają się one szczególnie do barwienia bawełny i podobnie jak barwniki kadziowe są redukowane do postaci rozpuszczalnej w wodzie za pomocą sody kaustycznej i ditioninów lub siarczku sodu ( związek leuko ), a po przyłączeniu do włókna utrwalane są na włóknie nierozpuszczalnie przez utlenianie . Ze względów toksykologicznych i ekologicznych obecnie w dużej mierze unika się utleniania dwuchromianem i coraz częściej stosuje się barwniki siarkowe o niskiej zawartości siarczków i bezsiarczkowych środków redukujących. Ze względu na niskie koszty produkcji barwniki siarkowe nadal odgrywają ważną rolę ilościową. Barwniki siarkowe są szczególnie zmywalne i odporne na światło, kolory są zwykle stonowane.
Klasyfikacja według technologii aplikacji
Podczas gdy niuans koloru barwnika jest zasadniczo determinowany przez chromofor, właściwości barwników można zmieniać, wprowadzając odpowiednie grupy chemiczne w taki sposób, że różne typy substratów mogą być barwione. Skutkuje to klasyfikacją różnych barwników zgodnie z procesem barwienia. Po tej klasyfikacji następuje również wskaźnik barwny , ważny standard pracy w dziedzinie chemii barwników. Na podstawie wskaźnika koloru (CI) farbiarz może zidentyfikować klasę barwnika, kolor i substancję. CI zawiera ponad 10 000 barwników - ponad 50% z nich to barwniki azowe.
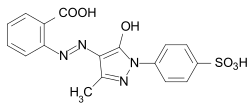
Barwniki zaprawowe
Nazwa pochodzi od procesu barwienia, w którym na zaplamiony materiał nanosi się odpowiednie barwniki kwasowe – głównie wełnę i jedwab. W celu barwienia barwnikami bejcowymi, farbowane włókna są najpierw poddawane obróbce solami chromu (III), żelaza (III) lub glinu i barwione. Podczas późniejszej obróbki parą na włóknie tworzą się wodorotlenki metali. Podczas barwienia te wodorotlenki reagują z (najczęściej specjalnym) barwnikiem kwasowym, tworząc barwnik metalokompleksowy . Proces na włóknie odpowiada lakierowaniu .
Jeśli stosuje się sole chromu, mówi się o barwnikach chromujących. W zależności od rodzaju barwnika , sól chromu – zwykle chromiany lub dichromiany – można dodać przed, w trakcie lub po barwieniu. W związku z tym rozróżnia się procesy chromowania przed, po i w jednej kąpieli. Barwniki chromujące wyróżniają się szczególnie dobrą odpornością na wilgoć. Jednak zanieczyszczenie metalami ciężkimi włókien i ścieków farbiarskich jest niekorzystne i krytyczne z ekologicznego punktu widzenia.
Barwniki do bejcowania są oznaczane jako barwniki CI Mordant zgodnie ze wskaźnikiem barw .
Przykłady:
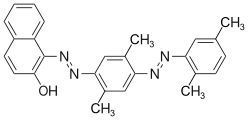
Barwniki bezpośrednie
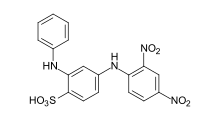
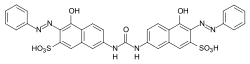
Ze względu na wysoką substantywność, barwniki bezpośrednie (lub barwniki rzeczownikowe) są wchłaniane bezpośrednio z roztworu wodnego na włókno. Nadają się szczególnie do stosowania na celulozie . Barwniki te są wiązane z włóknem poprzez interakcje fizyczne ( wiązania van der Waalsa ). Większość przedstawicieli pochodzi z grupy barwników azowych, najlepiej barwników poliazowych.
Barwniki bezpośrednie są określane jako barwniki bezpośrednie CI zgodnie ze wskaźnikiem koloru .
Przykłady:
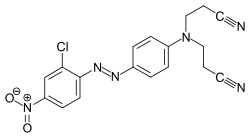
Barwniki dyspersyjne
Prawie nierozpuszczalne w wodzie barwniki dyspersyjne są korzystnie stosowane do barwienia hydrofobowych włókien poliestrowych i octanowych . Są one bardzo drobno zmielone razem z dyspergatorami , co oznacza, że rozpuszczone molekularnie składniki barwnika mogą dyfundować do włókna podczas procesu barwienia, gdzie tworzą stały roztwór, co powoduje, że barwniki są zmywalne i odporne na działanie światła.
Zdecydowana większość barwników dyspersyjnych należy do barwników azowych. Ze względu na wysoką jakość mechanicznie włókien poliestrowych, barwniki dyspersyjne stanowią bardzo ważną grupę barwników. Całkowita wartość sprzedaży w 1999 roku dla Europy Zachodniej wyniosła 98 milionów euro.
Barwniki dyspersyjne są określane jako barwniki dyspersyjne CI zgodnie ze wskaźnikiem barw .
Przykłady:
Barwniki rozwijające lub sprzęgające
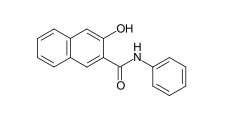
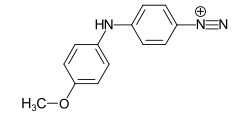
W przypadku wywoływania barwników barwnik praktycznie nierozpuszczalny w wodzie powstaje bezpośrednio na włóknie w reakcji rozpuszczalnego w wodzie składnika sprzęgającego ( CI Azoic Coupling Component ) z rozpuszczalnym w wodzie dwuazowym składnikiem ( CI Azoic Diazo Component ). Ta klasa barwników stosowana jest głównie do barwienia włókien celulozowych, których wybarwienia charakteryzują się bardzo dobrą odpornością na wilgoć. Najważniejszym składnikiem sprzęgającym w barwnikach wywołujących jest CI Coupling Component 2 (Naphthol AS) .
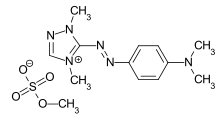
Barwniki kationowe
Barwniki kationowe to dodatnio naładowane związki, które w połączeniu z włóknami poliakrylonitrylowymi (PAN) i anionowo modyfikowanym poliestrem dają błyszczące i odporne na światło kolory. Tworzą wiązania jonowe z ujemnie naładowanymi grupami na włóknie. Do barwników kationowych można stosować różne chromofory, przy czym ładunek dodatni w barwnikach metinowych ulega delokalizacji w przeciwieństwie do innych systemów chromoforowych.
Nawet jeśli barwniki kationowe są nazwane według wskaźnika barwy z barwnikami podstawowymi CI , termin barwniki podstawowe dla tej grupy barwników nie jest już używany w nowszej literaturze.
Barwniki kadziowe
Barwniki kadziowe obejmują nierozpuszczalne w wodzie barwniki, które zostały wniesione w swojej rozpuszczalnej dihydro lub leuko forma przez redukcję ( kadziowania ) w alkalicznym roztworze do barwienia . Anion wykazuje wystarczające powinowactwo do włókien bawełny lub wiskozy, aby można było wchłonąć barwnik kadziowy. Tutaj jest on ponownie przekształcany w stan nierozpuszczalny przez kolejne utlenianie . Można to zrobić za pomocą tlenu atmosferycznego lub obróbki środkami utleniającymi. Barwnik jest quasi molekularnie związany z włóknem, to „wytrącanie we włóknie” powoduje wysoką pranie i odporność na światło. Nierozpuszczalne w wodzie barwniki siarkowe zachowują się również jak barwniki kadziowe.
Najważniejszym barwnikiem kadzi jest indygo . W indantren są również ważne.
Barwniki kadziowe są oznaczone jako barwniki kadziowe CI zgodnie ze wskaźnikiem barw .
Przykłady:
Barwnik spożywczy
Barwniki spożywcze są stosowane jako dodatki do żywności w celu skompensowania zmian koloru związanych z przetwarzaniem lub spełnienia wymagań kolorystycznych konsumentów. Stosowane są zarówno barwniki pochodzenia naturalnego, jak i barwniki produkowane syntetycznie. Stosowanie barwników jak barwnik spożywczy jest ściśle regulowane przez prawo - w UE przez rozporządzenie (WE) nr 1333/2008 z dnia 16 grudnia 2008 roku w sprawie dodatków do żywności. Na rynek mogą być wprowadzane tylko zatwierdzone dodatki do żywności z numerem E. Te dodatki muszą być oznaczone na produkcie.
Barwniki spożywcze są określane jako barwniki spożywcze CI zgodnie ze wskaźnikiem barwy .
Barwniki rozpuszczalnikowe
Barwniki rozpuszczalnikowe , nazwane zgodnie z Color Index Solvent Dyes , to nierozpuszczalne w wodzie barwniki, które są rozpuszczalne w różnych rozpuszczalnikach organicznych, takich jak alkohole, estry czy węglowodory. Z reguły struktury barwników rozpuszczalnikowych nie zawierają żadnych grup kwasu sulfonowego ani karboksylowych. Barwniki kationowe z wewnątrzcząsteczkową grupą sulfonianową lub karboksylanową jako przeciwaniony są wykluczone. Reprezentantów barwników rozpuszczalnikowych można znaleźć w różnych klasach barwników chemicznych, od barwników azowych, barwników antrachinonowych, barwników metalokompleksowych po ftalocyjaniny. Barwniki rozpuszczalnikowe stosowane są jako składnik lakierów (przykład: barwniki do lakierów zaponowych ), do barwienia produktów olejów mineralnych ( barwniki Sudan ), wosku , tuszy i różnych przezroczystych tworzyw sztucznych.
Barwniki rozpuszczalnikowe są określane jako barwniki rozpuszczalnikowe CI zgodnie ze wskaźnikiem barw .
Przykłady:
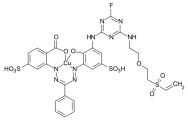
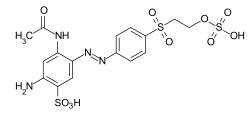
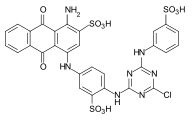
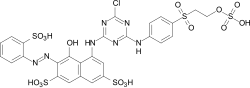
Barwniki reaktywne
Podczas procesu barwienia barwniki reaktywne tworzą wiązanie kowalencyjne z grupami funkcyjnymi włókna , co skutkuje barwieniem na mokro. Stanowią najliczniejszą grupę barwników do barwienia celulozy, ale można je również stosować do barwienia wełny i poliamidu w głębokich odcieniach.
Z chemicznego punktu widzenia barwniki reaktywne składają się z dwóch części - chromoforu i jednej lub więcej grup reaktywnych, znanych również jako reaktywne kotwice. Ważne są dwa różne systemy kotew reaktywnych:
- Związki heterocykliczne, na przykład podstawione halogenem pochodne triazyny lub pirymidyny . Podczas procesu barwienia reagują one z grupami hydroksylowymi włókien, odszczepiając halogenek wodoru i tworząc trwałe kowalencyjne wiązanie eterowe :
- Tak zwana grupa sulfonu winylowego , która reaguje z grupami nukleofilowymi włókna podczas procesu barwienia w sensie dodatku Michaela . Również w tym przypadku powstaje trwałe wiązanie eterowe. W przypadku wielu barwników winylosulfonowych, grupa winylosulfonowa jest w postaci zabezpieczonej jako półester kwasu siarkowego. Grupa winylosulfon jest tylko utworzone przez eliminację z kwasem siarkowym , zgodnie z zasadowych środków barwiących .
Te dwa typy reaktywnych kotwic mogą również występować równolegle w reaktywnym barwniku.
Jako chromofor, barwniki azowe są zdecydowanie najbardziej powszechne wśród barwników reaktywnych. Jednak ważną rolę odgrywają również inne układy chromoforowe, takie jak barwniki antrachinonowe, formazanowe i ftalocyjaniny.
Barwniki reaktywne są określane jako barwniki reaktywne CI zgodnie ze wskaźnikiem barw .
Przykłady:
Barwniki kwasowe
Barwniki kwasowe posiadają hydrofilowe , anionowe podstawniki – z reguły są to grupy kwasu sulfonowego. Większość przedstawicieli tej klasy barwników należy do barwników azowych, ale są też barwniki kwasowe z innymi chromoforami. Stosowane są głównie do barwienia wełny, jedwabiu i poliamidu, proces barwienia odbywa się w zakresie pH 2-6. Jeśli stosuje się małe cząsteczki barwnika, uzyskuje się jednolite wybarwienia, w których cząsteczki barwnika tworzą głównie wiązania podobne do soli z grupami amonowymi włókna. W przypadku tych produktów wymywanie ( odporność na wilgoć ) jest raczej umiarkowane. Wraz ze wzrostem wielkości cząsteczki wzrasta wiązanie barwnika poprzez siły adsorpcyjne pomiędzy hydrofobową częścią cząsteczki barwnika a włóknem. Poprawia to trwałość na mokro, ale w wielu przypadkach kosztem równomierności (wyrównania) barwienia.
Barwniki kwasowe są określane jako barwniki kwasowe CI zgodnie ze wskaźnikiem barwy .
Przykłady:
CI Acid Blue 3 ( błękit patentowy V )
Barwniki funkcjonalne
Podczas gdy konwencjonalne barwniki są używane, na przykład, do zmiany wyglądu tekstyliów, skóry i papieru, barwniki funkcjonalne na ogół nie mają zastosowania estetycznego. Typowe obszary zastosowania to barwniki wskaźnikowe lub barwniki zależne od napięcia
Specjalne barwniki mogą
- Pochłaniają światło o określonej długości fali i zamieniają pochłonięte światło na ciepło (np. w analizie chemicznej i biochemicznej),
- ponownie emitować światło o innej długości fali (jako biomarkery fosforescencyjne lub atramenty, fluorescencja w laserach barwnikowych, chemiluminescencja w celu zerwania lub przywrócenia wiązań chemicznych w biochemii),
- zmienić kierunek polaryzacji światła (jak przy podwojeniu częstotliwości lub jako przełącznik optyczny),
- powodować zjawiska elektryczne (stosowane w drukarkach laserowych),
- umożliwiają procesy fotochemiczne.
Z ekonomicznego punktu widzenia szczególnie ważne jest stosowanie barwników funkcjonalnych do produkcji płyt CD i DVD. Cząsteczki barwnika zawarte są w poliwęglanie płyty CD lub DVD. Cząsteczki barwnika absorbują energię świetlną poprzez wiązkę laserową palnika i przekształcają ją w ciepło. W wyniku absorpcji ciepła w tym miejscu topi się tworzywo sztuczne, czyli poliwęglan. Powierzchnia nieznacznie się zmieniła, zmieniona struktura powierzchni jest postrzegana podczas procesu odczytu.
Produkcja barwników przemysłowych
Oprócz reakcji chemicznych przemysłowa produkcja barwników obejmuje różne procesy fizyczne, takie jak wysalanie , filtracja , odwrócona osmoza (RO) , suszenie i mielenie.
Przed lub po suszeniu handlowe barwniki są standaryzowane pod kątem określonej intensywności koloru poprzez dodanie bezbarwnych, obojętnych środków regulujących, takich jak siarczan sodu, chlorek sodu lub dekstryna, w celu skompensowania wahań w różnych partiach produkcyjnych. Celowe dodawanie innych barwników (barwników cieniujących) może zapewnić, że produkt handlowy pozostanie stały w kolorze. Trwałość produktów podczas przechowywania można w niektórych przypadkach zwiększyć przez dodanie substancji buforowych, takich jak fosforan jedno- i dwusodowy .
Szczególnie w przypadku barwników słabo rozpuszczalnych w wodzie, szlifowanie ma duży wpływ na proces barwienia (odcień, siła koloru ). W latach sześćdziesiątych i siedemdziesiątych oprócz proszków barwiących wprowadzano na rynek coraz bardziej stężone wodne roztwory barwników. Wraz z wprowadzeniem marek płynnych, takich jak opracowanie granulatów barwników, ułatwiono automatyczne dozowanie barwników w farbiarni i zmniejszono zanieczyszczenie pyłem.
Przed 1980 rokiem przemysłowa produkcja barwników była bardzo silna w Europie Zachodniej, Ameryce Północnej i Japonii. Rosnące koszty ochrony środowiska i rosnąca presja importu z Azji przez wielu nietradycyjnych producentów barwników, zwłaszcza z Chin, Indii, Korei i Tajlandii, doprowadziły do znacznej restrukturyzacji wśród producentów tradycyjnych barwników. Biznes barwników został skoncentrowany poprzez przejęcia i wspólne przedsięwzięcia, w wyniku których wiele zakładów produkcyjnych zostało zamkniętych.
Dużymi tradycyjnymi producentami barwników są Huntsman (dawniej Ciba ), DyStar (powstały z działów barwników Hoechst AG , Bayer AG i BASF ) oraz Archroma (powstały z Clariant ). Ci tradycyjni producenci barwników produkują obecnie głównie w Azji.
Zobacz też
- Lista barwników posortowana według koloru
- Barwienie w czasach starożytnych
literatura
- Heinrich Zollinger: Chemia kolorów: synteza, właściwości i zastosowania organicznych barwników i pigmentów . 3. Wydanie. WILEY-VCH Verlag, Weinheim 2003, ISBN 3-906390-23-3 ( ograniczony podgląd w wyszukiwarce książek Google).
- Klaus Hunger (red.): Barwniki przemysłowe: chemia, właściwości, zastosowania . WILEY-VCH Verlag, Weinheim 2003, ISBN 3-662-01950-7 ( ograniczony podgląd w wyszukiwarce książek Google).
- Jürgen Fabian, Horst Hartmann: Absorpcja światła organicznych barwników. Ujęcie teoretyczne i reguły empiryczne . Springer, Berlin 1980, ISBN 3-642-67589-1 ( ograniczony podgląd w wyszukiwarce książek Google).
- Martin Klessinger: Budowa i absorpcja światła barwników organicznych . W: Chemia naszych czasów . taśma 12 , 1978, s. 1-11 .
- Guido Ebner, Dieter Schelz: Barwienie tkanin i barwniki . Springer-Verlag, Berlin 1989, ISBN 3-642-70172-8 ( ograniczony podgląd w wyszukiwarce książek Google – przedruk 2011).
- Wilfried Kratzert, Rasmus Peichert: Barwniki . Quelle i Meyer, Heidelberg 1981, ISBN 3-494-01021-8 .
- Helmut Schweppe: Podręcznik naturalnych barwników. Wystąpienie - użycie - dowód . ecomed, Landsberg / Lech 1993, ISBN 3-609-65130-X .
- Lutz Roth, Kurt Kormann, Helmut Schweppe: Rośliny barwiące - barwniki roślinne. Botanika - metody barwienia - analizy - tureckie dywany i ich motywy . Ecomed, Landsberg / Lech 1992, ISBN 3-609-65490-2 .
- Sabine Struckmeier: Barwniki naturalne: kolory z historią . W: Chemia naszych czasów . taśma 37 , nie. 6 , 2003, s. 402-409 , doi : 10.1002 / ciuz.200300275 .
- Herbert Vogler: Barwienie trwa od tysięcy lat – przegląd starożytnego barwienia . W: wykańczanie tekstyliów . taśma 21 , nie. 6 , 1986, s. 229-235 .
- Herbert Vogler: 150 lat przemysłu farbiarskiego. Część I . W: wykończenie tekstyliów . taśma 42 , nie. 11.12.2007 , s. 11-14 ( tib.eu ).
- Herbert Vogler: 150 lat przemysłu farbiarskiego. Część II . W: wykończenie tekstyliów . taśma 43 , nie. 1/2 , 2008, s. 10-14 ( tib.eu ).
- Anthony Travis: Twórcy tęczy: pochodzenie przemysłu barwników syntetycznych w Europie Zachodniej . Lehigh Univ. Prasa, Betlejem / Londyn / Toronto 1993, ISBN 0-934223-18-1 .
linki internetowe
- Thomas Seilnacht: Leksykon pigmentów i barwników na seilnacht.com, dostęp 7 stycznia 2017 r.
- Lexicon of Dye Plants na digitalefolien.de, dostęp 7 stycznia 2017 r.
- J. Scherkenbeck: Barwniki ( Pamiątka z 8 stycznia 2017 w Internet Archive ) (PDF; 2,16 MB)
Indywidualne dowody
- ↑ DIN 55943 . W: Niemiecki Instytut Normalizacyjny odc. V. (red.): Barwniki 1 . Wydanie siódme. DIN-Taschenbuch 49.Berlin, Wiedeń, Zurych 2012, ISBN 978-3-410-23202-5 , s. 509 .
- ↑ a b c Wolfgang Glöckner, Walter Jansen, Rudolf G. Weißenhorn (red.): Podręcznik chemii doświadczalnej, poziom II, tom 10, Aulis Verlag Deubner & Co. KG, Kolonia 2008, ISBN 978-3-7614-2388 -2 , str. 304-309.
- ^ B c Christian-Herbert Fischer: barwniki historyczne . W: Spektrum nauki . nr 10, 1997, s. 104 i n.
- ↑ Encyklopedia chemii technicznej Ullmanna . Wydanie IV. Tom 11, słowo kluczowe: barwniki naturalne. s. 103.
- ^ Karl Aloys Schenzinger: Anilina. Zeitgeschichte-Verlag Berlin, 1937, OCLC 6866470 .
- ↑ George B. Kauffman: Pittacal - Pierwszy syntetyczny barwnik. W: Journal of Chemical Education. 54, 1977, s. 753, doi: 10.1021 / ed054p753 .
- ^ Karl Huebner: Historia: 150 lat Mauvein . W: Chemia naszych czasów . taśma 40 , nie. 4 , 2006, s. 274–275 , doi : 10.1002 / ciuz.200690054 .
- ↑ Hans Joachim Störig : Mała światowa historia nauki 2. 4. Wydanie. Fischer Taschenbuch, 1982, ISBN 3-596-26399-9 , s. 136-137.
- ↑ a b Hermann Raaf: Chemia organiczna w szkle testowym. Wydanie 13, Kosmos Verlag, Stuttgart 1975, ISBN 3-440-04266-9 , s. 186.
- ↑ Joachim Rudolf: Księga współczesnej chemii Knauera. Th. Knauer Nachf., Monachium/Zurych 1975, ISBN 3-426-00381-3 , s. 257-263.
- ↑ a b c 1865-1901: Wiek kolorów . basf.pl. Źródło 9 listopada 2018.
- ↑ Renate Kaiser-Alexnat: Indygo - Król Barwników . W: Magazyn Azji Południowo-Wschodniej . Wydanie 3, 2008 ( ograniczony podgląd w Google Book Search).
- ↑ Ernst Bäumler: Czerwona fabryka . R. Piper GmbH & Co. KG, Monachium 1988, ISBN 3-492-10669-2 .
- ↑ Historia firmy Bayer AG , dostęp 8 listopada 2018 r.
- ↑ Werner Abelshauser (red.): BASF: historia firmy . Wydanie II. CH Beck, Monachium 2003, ISBN 3-406-49526-5 ( ograniczony podgląd w wyszukiwarce książek Google).
- ^ B Klaus Hunger (Ed.): Barwniki przemysłowe: Chemistry, Properties, Applications . WILEY-VCH Verlag, Weinheim 2003, ISBN 978-3-662-01950-4 ( ograniczony podgląd w wyszukiwarce książek Google).
- ↑ John Griffiths: Barwniki funkcjonalne. Nowy trend w chemii barwników . W: Chemia naszych czasów . taśma 27 , nie. 1 . Wiley-VCH Verlag, Weinheim 1993, s. 21-31 , doi : 10.1002 / ciuz.19930270104 .
- ↑ Barwniki funkcjonalne - Od korzeni chemii barwników do produktów wysokochemicznych . chemanager-online.com. Źródło 13 listopada 2018.
- ↑ K. Peter C. Vollhardt: Chemia organiczna. VCH, Weinheim, wydanie 1 1988, s. 618, ISBN 3-527-26912-6 .
- ↑ Wpis dotyczący barwników cyjaninowych. W: Rompp Online . Georg Thieme Verlag, dostęp 4 lutego 2019 r.
- ↑ Wpis dotyczący barwników triarylometanowych. W: Rompp Online . Georg Thieme Verlag, dostęp 14 stycznia 2019 r.
- ^ B Heinrich Zollingera: Chemistry Kolor: Synteza, właściwości i zastosowania organicznych barwników i pigmentów . 3. Wydanie. WILEY-VCH Verlag, Weinheim 2003, ISBN 3-906390-23-3 ( ograniczony podgląd w wyszukiwarce książek Google).
- ↑ Wpis dotyczący barwników siarkowych. W: Rompp Online . Georg Thieme Verlag, dostęp 14 stycznia 2019 r.
- ↑ Kirk-Othmer, Jacqueline I. Kroschwitz: Encyklopedia Technologii Chemicznej. wydanie 5, t. 9, 2005, ISBN 978-0-471-48494-3 , s. 349.
- ↑ P. Rys, G. Zollinger: Przewodnik po chemii barwników. Wydanie drugie, Verlag Chemie, Weinheim 1976, ISBN 3-527-25650-4 , s. 181, 182.
- ↑ Wpis dotyczący barwników chromujących. W: Rompp Online . Georg Thieme Verlag, dostęp 23 stycznia 2019 r.
- ↑ Bertram Philipp, Peter Stevens Podstawowe cechy chemii przemysłowej. VCH Verlagsgesellschaft mbH, 1987, ISBN 3-527-25991-0 , s. 321.
- ^ Wittko Francke, Wolfgang Walter: Podręcznik chemii organicznej. S. Hirzel Verlag, Stuttgart 2004, ISBN 3-7776-1221-9 , s. 684 f.
- ↑ Rozporządzenie (WE) nr 1333/2008 z dnia 16 grudnia 2008 r. w sprawie dodatków do żywności (PDF) , dostęp 5 sierpnia 2019 r.
- ↑ Zezwolenia i stosowanie dodatków do żywności. Federalne Ministerstwo Wyżywienia i Rolnictwa, dostęp 5 sierpnia 2019 r .
- ↑ H. Zollinger: Chemia barwników reaktywnych . W: Angew. Chem 73, nr 4, 1961, strony 125-136, doi: 10.1002/anie.19610730402 .
- ↑ a b c John Griffiths: Barwniki funkcjonalne. Nowy trend w chemii barwników . W: Chemia w naszych czasach. 27, nr 1, 1993, s. 21-31, doi: 10.1002/ciuz.19930270104 .
- ↑ Klaus Roth: Chemia olśniewających płyt: CD, DVD & Co. W: Chemia w naszych czasach. 41, nr 4, 2007, s. 334-345, doi: 10.1002 / ciuz.200700428 .
- ^ Hermann Rath: Podręcznik chemii włókienniczej . w tym tekstylna technologia chemiczna. Wydanie II. Springer-Verlag, Berlin, Heidelberg 1963, ISBN 978-3-662-00065-6 , s. 455 ( ograniczony podgląd w wyszukiwarce Google Book).
- ^ B Roland Dittmeyer Wilhelm Keim Gerhard Kreysa Karl Winnacker Leopold Küchler: Chemical Technology, procesów i produktów. Tom 7, Produkty przemysłowe, wydanie 5.. Wiley-VCH Verlag GmbH & Co. KGaA, 2004, ISBN 3-527-30772-9 , s. 397 ff.