Monosacharydy
Monosacharydy ( stara gr . Μόνος mónos „sam”, τό σάκχαρ tó sákchar „cukier” i -ειδής -eidés „podobne, kształtowane”, zwane także cukrami prostymi ) to grupa związków organiczno-chemicznych . Są produktami częściowego utleniania alkoholi wielowodorotlenowych. Wszystkie monosacharydy mają łańcuch z co najmniej trzech atomów węgla jako podstawową strukturę i mają grupę karbonylową i co najmniej jedną grupę hydroksylową . Są budulcem wszystkich węglowodanów i mogą łączyć się, tworząc disacharydy ( podwójne cukry ), oligosacharydy ( wiele cukrów ) lub polisacharydy ( wiele cukrów ).
Monosacharydy glukoza , fruktoza i galaktoza są najważniejszymi cukrami w metabolizmie . Są nośnikami energii, a także służą jako elementy budulcowe komórek.
budowa
Każdy cukier prosty składa się z łańcucha atomów węgla. Łańcuch może być otwarty ( niecykliczny) lub zamknięty w pierścieniu (cykliczny) .
Ze względu na liczbę atomów węgla mówi się o diozach (2), triozy (3), tetrozach (4), pentozach (5), heksozach (6), heptozach (7) itd. Najmniejsze cukry proste, czyli trioza , mają trzy atomy węgla. W zasadzie długość łańcucha węglowego jest nieograniczona, ale dotychczas w naturze obserwowano tylko cukry proste zawierające maksymalnie dziewięć atomów węgla, przy czym najczęściej występowały heksozy i pentozy.
Ponadto jeden z atomów węgla w postaci niecyklicznej (z otwartym łańcuchem) ma podwójnie związany atom tlenu , tj. Grupę karbonylową. Jeśli grupa karbonylowa znajduje się na końcu łańcucha węglowego, grupę tę określa się jako grupę aldehydową, a cukier jako aldozę , w przypadku grupy karbonylowej w łańcuchu z grupy ketonowej oraz w przypadku cukru z ketoz .
Obie nomenklatury mogą być używane razem, tak że cukier prosty z sześcioma atomami węgla i jedną grupą aldehydową nazywany jest aldoheksozą.
Dla każdego monosacharydu o otwartym łańcuchu o wystarczającej długości istnieją formy cykliczne, z zamknięciem pierścienia od grupy karbonylowej do grupy hydroksylowej (grupa OH). Pierścień składa się zatem z atomów węgla i jednego atomu tlenu. Rozróżnia się furanozy (pięć pierścieni) i piranozy (sześć pierścieni). Cykliczne monosacharydy pochodzące od aldoz to półacetale pochodzące z ketoz hemiketali .
W najprostszych przedstawicielach monosacharydów, każdy z pozostałych atomów węgla bez grupy karbonylowej ma grupę hydroksylową (grupę OH), a poza tym atomy wodoru. Ogólny wzór dotyczy tych związków : C n H 2n O n .
Jednakże pochodne tych prostych związków należą również do monosacharydów, takich jak aminocukry (np glukozaminy ) i deoxysugars (np deoksyrybozy ). Nie odpowiadają one tej ogólnej formule empirycznej.
Struktura przestrzenna
Oprócz pozycji grupy karbonylowej ( grupy okso) w łańcuchu węglowym ważną rolę odgrywa również rozmieszczenie przestrzenne grup OH. Na przykład w przypadku aldoheksozy można rozróżnić cztery atomy węgla w zależności od „prawej” lub „lewej” grupy OH. Istnieje zatem łącznie 16 (2 4 = 16) różnych stereoizomerów aldoheksozy, które różnią się pod względem metabolizmu i aktywności optycznej . Ponadto liczba teoretycznie możliwych stereoizomerów wzrasta pięciokrotnie, ponieważ oprócz postaci z otwartym łańcuchem, w wyniku wewnątrzcząsteczkowego tworzenia cyklicznego półacetalu może powstać również postać furanozy lub piranozy o konfiguracji α lub β.
Reprezentację stereochemiczną można wykonać na trzy równe sposoby. Najstarszym przedstawieniem jest rzut Fischera , w którym wszystkie wiązania CC są zapisane w wyimaginowanym (najbardziej niekorzystnym termodynamicznie) położeniu zaćmienia pionowo jedno nad drugim i rozwinięte na płaszczyźnie papieru. Te podstawniki , tutaj atomów wodoru i grup hydroksylowych, są wymienione w prawo lub w lewo zależnie od konfiguracji i znajdują się powyżej płaszczyzny papieru, tak, że jasne wyniki konfiguracji. Grupa hydroksylowa chiralnego atomu C znajdująca się najdalej od anomerycznego atomu C tworzy konfigurację D w pozycji prawej i konfigurację L w pozycji lewej (patrz przykład rybozy D i L powyżej).
Cykliczny półacetal jest mylący w przedstawieniu ( 1 ), który jest również nazywany wzorem pierścienia Tollensa i wymagane są zbyt długie wiązania. W związku z tym opracowano dalsze reprezentacje. Przedstawienie Hawortha ( 2 ) odpowiada projekcji Fischera „położonej na boku” i zwiniętej. Wszystkie atomy pierścienia są na jednym poziomie, wrażenie przestrzenne można wzmocnić wiązaniami perspektywicznymi. Wiązanie podstawnika „w górę” ma wskazywać, że znajduje się on powyżej płaszczyzny pierścienia. Grupy skierowane w lewo (lub w prawo) w rzucie Fischera wskazują w górę (lub w dół) na Haworth-Ring.
Wzór konformacyjny ( 3 ) jest jeszcze bardziej realistyczny , ponieważ można tu zobaczyć kątowe ułożenie łańcucha węglowego. Reprezentacja stereochemiczna ( 4 ) jest również powszechna.
Ważne monosacharydy
Drzewo genealogiczne aldoz
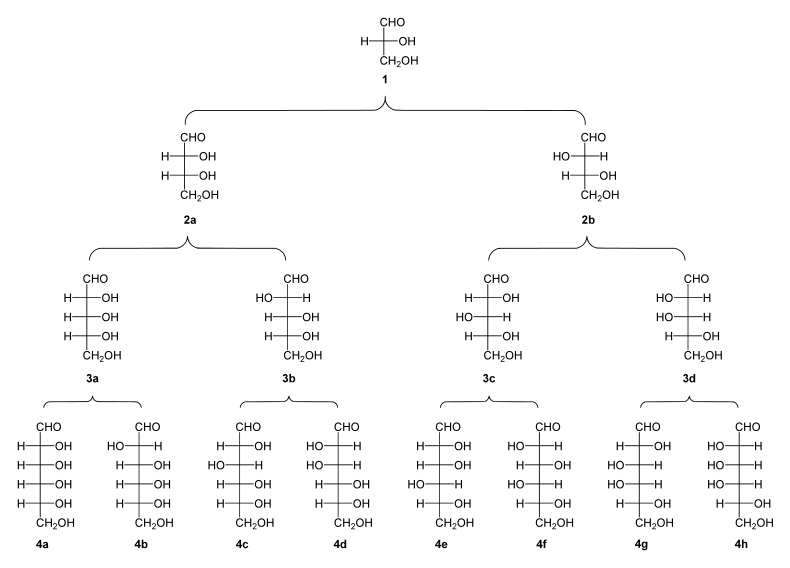
( 1 ) D - (+) - gliceraldehyd ;
( 2a ) D - (-) - erytroza ; ( 2b ) D - (-) - treoza ;
( 3a ) D - (-) - ryboza ; ( 3b ) D - (-) - arabinozy ; ( 3c ) D - (+) - ksyloza ; ( 3d ) D - (-) - leksoza ;
( 4a ) D - (+) - alloza ; ( 4b ) D - (+) - róża altowa ; ( 4c ) D - (+) - glukoza ; ( 4d ) D - (+) - mannoza ; ( 4e ) D - (-) - guloza ; ( 4f ) D - (-) - idoza ; ( 4g ) D - (+) - galaktoza ; ( 4h ) D - (+) - taloza
Rodowód ketoz

( 1 ) dihydroksyaceton ;
( 2 ) D - erytruloza ;
( 3a ) D - rybuloza ; ( 3b ) D - ksyluloza ;
( 4a ) D - psikoza ; ( 4b ) D - fruktoza ; ( 4c ) D - sorboza ; ( 4d ) D - Tagatoza
Trio
-
Aldotrioza
- D - i L - gliceraldehyd ( produkty przemiany materii )
-
(Ketotrioza)
- ( Dihydroksyaceton ) (Ponieważ dihydroksyaceton nie ma stereocentrum, w rzeczywistości nie jest uważany za monosacharyd. Jest jednak zaangażowany i ważny w metabolizmie węglowodanów).
Tetroses
- Aldotetrose
-
Ketotetrose
- D - erytruloza ( produkt przemiany materii)
Pentozy
-
Aldopentoza
- D - ryboza (występuje m.in.w RNA )
- D - i L - arabinoza (występująca m.in. w oligosacharydach roślinnych)
- D - ksyloza (także cukier drzewny, główny składnik hemiceluloz )
- D - Lyxosis (nie występuje w naturze)
- D - dezoksyryboza (występuje m.in.w DNA )
-
Ketopentoza
- D - rybuloza (produkt metaboliczny)
- D - i L - ksyluloza (pierwsza jest częścią szlaku pentozofosforanowego , druga metabolizmu glukuronianu)
Heksozy
-
Aldoheksozy
- D - Allose (bardzo rzadki w przyrodzie)
- D - Altrose (nie występuje w naturze, L-Altrose została znaleziona w bakterii)
- D - glukoza (także cukier gronowy, najczęściej monosacharyd)
- D - mannoza (zwykły monosacharyd)
- D - Gulose (rzadki w naturze, głównie w kształcie litery L)
- D - Idoza (nie występuje w naturze, ale odpowiadający mu kwas uronowy, kwas iduronowy , występuje głównie w glikozaminoglikanach )
- D - galaktoza (także cukier śluzowy, monosacharyd pospolity)
- D - Taloza (bardzo rzadko, część higromycyny antybiotyku tworzonej przez paciorkowce )
-
inne fizjologicznie ważne heksozy
- Kwas D - glukuronowy (6-karboksy- D- glukoza, często występuje zwykle w postaci glukuronianu lub estryfikacji )
- Kwas D - galakturonowy (6-karboksy- D- galaktoza, występuje zwykle w postaci uronianu lub estryfikacji)
- N -acetylo-D-glukozamina (również N- acetylochitozamina, monomer chityny , jest szeroko rozpowszechniona)
- D - glukozamina (także chitozamina, monomer chitozanu )
- N -acetylo-D-galaktozamina (również N- acetylochondroamina, jest szeroko rozpowszechniona)
- D - a zwłaszcza L - fukozy (6-deoksy- D - i - L- galaktoza, ta ostatnia jest szeroko rozpowszechniona)
- L - ramnoza (6-deoksy- L- mannoza, występuje w oligosacharydach roślinnych)
- D - Chinovose (6-deoksy- D -glukoza, występuje m.in. w oligosacharydach roślinnych)
-
Ketoheksozy
- D - fruktoza (także cukier owocowy, monosacharyd pospolity)
- Rzadkie heksozy
Wyższe monosacharydy
- D - sedoheptulozę (C 7 keto-cukru, występuje jako 7-fosforanu w pentozy fosforan ścieżka )
- Kwas 3-deoksy-D- manno -okt-2-ulosonowy (również kwas 2-keto-3-deoksyoktonowy, KDO, cukier C 8 , ważny składnik lipopolisacharydów na powierzchni komórek niektórych bakterii)
- D - kwas sialowy (również N- acetylo-neuraminowy kwas , C 9 cukier ketonową, odgrywa rolę w ujęciu komórka-komórka w glikokoniugatów )
fotosynteza
Punktem wyjścia dla większości cukrów prostych w organizmach żywych jest fotosynteza tlenowa . Podczas tego procesu przy użyciu energii słonecznej cukier powstaje z CO 2 ( dwutlenek węgla ) i atomów wodoru zawartych w H 2 O ( wodzie ) . Kiedy woda jest rozszczepiana, tlen jest uwalniany jako produkt odpadowy .
Proste cukry w żywności
Cukry proste występują jako glukoza (cukier winogronowy) i fruktoza (cukier owocowy) w produktach spożywczych, takich jak owoce, miód i słodycze. Galaktozy , zwany cukier śluz w mleku, jest cukrem prostym. Natomiast cukry trzcinowe , mleczne lub słodowe są podwójnymi cukrami; Skrobia i glikogen to polisacharydy. Wszystkie wyższe cukry muszą najpierw zostać rozbite na rozpuszczalne w wodzie di- lub monosacharydy, aby mogły zostać wchłonięte do krwi lub przetransportowane do wątroby za pośrednictwem białek transportowych - takich jak transporter glukozy - lub zwykłej dyfuzji.
Doustne spożycie cukrów prostych, glukozy i galaktozy, prowadzi do szybkiego wzrostu poziomu cukru we krwi ; wszystkie inne cukry proste są metabolizowane głównie w wątrobie i nie mają bezpośredniego wpływu na poziom glukozy we krwi. Ponieważ poziom cukru we krwi musi wahać się w wąskim zakresie, organizm musi przeciwdziałać szybkiemu wzrostowi poprzez szybkie dalsze przetwarzanie. Poziom insuliny wzrasta, a glukoza we krwi znajduje się w glikogenie wątroby - polisacharydzie przekształconym - z jednostek glukozy. Powoduje to szybki magazyn energii w wątrobie, ponieważ glikogen w razie potrzeby może zostać szybko ponownie rozłożony na glukozę. Nadmiar glukozy, który nie może być magazynowany jako glikogen, jest przekształcany w tkance tłuszczowej i wątrobie w triacyloglicerole ( tłuszcze ), które służą jako magazyn energii w wątrobie, mięśniach szkieletowych i komórkach tłuszczowych .
Dietetycy zalecają spożywanie maksymalnie 10% całkowitej ilości energii z cukrów prostych i podwójnych. Polisacharydy, takie jak v. za. Skrobie uważa się za lepiej nadaje się do spełniają wymagania węglowodanów, ponieważ muszą zostać najpierw za pomocą prostych cukrów w przewodzie pokarmowym, co prowadzi do znacznie wolniejsze wchłanianie węglowodanów.
literatura
- Gerhard Richter: Metabolic Physiology of Plants. Fizjologia i biochemia metabolizmu pierwotnego i wtórnego . Szóste, całkowicie poprawione wydanie. Georg Thieme, Stuttgart i in. 1998, ISBN 3-13-442006-6 , s. 213–223 ( ograniczony podgląd w wyszukiwarce Google Book).
linki internetowe
Indywidualne dowody
- ↑ Espacenet - Dane bibliograficzne. Źródło 18 listopada 2018 r .
- ↑ Hans-Dieter Belitz , Werner Grosch, Peter Schieberle : Podręcznik chemii żywności. Szóste, całkowicie poprawione wydanie. Springer, Berlin i in. 2008, ISBN 978-3-540-73201-3 , s. 895.
- ↑ Georg Löffler, Petro E. Petrides, Peter C. Heinrich (red.): Biochemistry and Pathobiochemistry. 8. całkowicie poprawione wydanie. Springer Medicine, Heidelberg 2007, ISBN 978-3-540-32680-9 .
- ^ Hermann Hager (założyciel), Hubert Schneemann, Gisela Wurm: Podręcznik praktyki farmaceutycznej Hagera. Dalsze prace, kontynuacja tom 1: Towary i usługi. Piąte, całkowicie poprawione wydanie. Springer, Berlin i in. 1995, ISBN 3-540-58958-9 , s. 18.
- ↑ Raport Organizacji Narodów Zjednoczonych ds. Wyżywienia i Rolnictwa : Dieta, odżywianie i zapobieganie chorobom przewlekłym (tabela 6)


