amalgamat
Amalgamatu ( starożytnego greckiego μαλακός malakos „miękkie” z alfa privativum tj „nie-zmiękczający”, zgodnie z innym etymology arabska in malagma „zmiękczający maści” lub al-magam z greckiego málagma ) jest stopu z rtęcią w chemii . Amalgamat w szerszym znaczeniu jest często także nieodwracalną mieszaniną innych substancji, zwykle stopem kilku metali. W sensie przenośnym amalgamat jest również mieszanką różnych terminów, idei, kultur lub tradycji.
Ponieważ wiele metali jest rozpuszczalnych w rtęci, istnieje bardzo wiele amalgamatów. Niektóre metale, takie jak żelazo, nie tworzą amalgamatu. Amalgamaty o wysokiej zawartości rtęci są często płynne, podobnie jak sama rtęć w temperaturze pokojowej ; jeśli zawartość rtęci jest niższa, są one stałe.
W klasycznej alchemii amalgamacja („koagulacja”) rtęci z innymi metalami jest często porównywana z połączeniem fizycznym. Jako alchemiczny leksem jest średniowieczna łacińska amalgama, którą zamieszkuje od XIII wieku.
Amalgamaty naturalne

Kilka naturalnie występujących amalgamatów jest znanych i uznanych przez Międzynarodowe Stowarzyszenie Mineralogiczne jako samodzielne minerały :
- Z ołowiem: amalgamat ołowiu (Pb 2 Hg)
- Z miedzią: Belendorffit (Cu 7 Hg 6 ), Kolymit (Cu 7 Hg 6 )
- Z palladem: Potarit (PdHg)
- Ze srebrem: eugenit (Ag 11 Hg 2 ), luanheit (Ag 3 Hg), moschellandsbergit (Ag 2 Hg 3 ), paraschachneryt (Ag 1,2 Hg 0,8 ), schachneryt (Ag 1,1 Hg 0,9 )
- Ze srebrem i złotem: Weishanite ((Au, Ag) 3 Hg 2 )
Amalgamaty techniczne i ich zastosowania
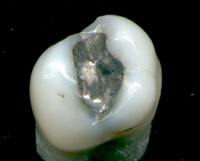
Amalgamat dentystyczny
W stomatologii jako materiał do wypełniania zębów szeroko stosuje się stop rtęci z innymi metalami, takimi jak srebro, miedź, ind, cyna i cynk. Nie udało się udowodnić związku z poważnymi problemami zdrowotnymi. Narażenie na rtęć jest minimalne.
Amalgamat sodu
Ważnym technicznie reduktorem w chemii organicznej i nieorganicznej oraz amalgamatem produkowanym na dużą skalę jest amalgamat sodowy , będący produktem pośrednim w wariancie elektrolizy chloro-alkalicznej . Rozkłada się wraz z wodą, tworząc sodę kaustyczną , wodór i rtęć , które są ponownie wykorzystywane do elektrolizy w obwodzie .
Amalgamat amonowy
Ponieważ metale alkaliczne tworzą amalgamaty, na przykład podczas elektrolizy roztworów jonów metali alkalicznych za pomocą elektrod rtęciowych, podjęto również próby wytworzenia amalgamatu amonowego lub amonowego (jon amonowy często zachowuje się podobnie do jonów metali alkalicznych); Natomiast amalgamat amonu rozkłada się na rtęć, amoniak i wodór .
Złoty amalgamat
Rtęć jest czasami nadal wykorzystywana w rzemieślniczym wydobyciu złota . Odpowiednie surowce zawierające złoto są mieszane lub ugniatane (łączenie) z ciekłą rtęcią. Tworzy to początkowo płynny amalgamat ze złotem, który występuje w małych płatkach lub granulkach w mielonej skale, prażonych koncentratach rudy lub w luźnych osadach z mydlanych osadów , które dzięki większej gęstości można łatwo oddzielić od lżejszych składników. Aby uzyskać z niego czyste złoto, amalgamat jest podgrzewany, dzięki czemu rtęć odparowuje; proces ten nazywany jest również paleniem. Powstają opary rtęci, które są niezwykle niebezpieczne dla zdrowia.
Amalgamaty złota są również wykorzystywane w złocnictwie chemicznym, znanym jako złocenie ogniowe . Złoty amalgamat jest nakładany lub malowany na metalowy przedmiot, a rtęć jest odparowywana pod wpływem ciepła.
Amalgamat aluminium
Jako środek redukujący stosuje się amalgamat glinu .
Amalgamat talu
Amalgamat talu ma niższą temperaturę topnienia -58 ° C niż czysta rtęć (-38,83 ° C) i dlatego - pomimo wysokiej toksyczności - jest używany jako płyn do termometrów do termometrów niskotemperaturowych.
Amalgamat cynku
Amalgamat cynku jest stosowany jako środek redukujący w organicznej chemii syntetycznej, zwłaszcza w redukcji Clemmensena do redukcji aldehydów lub ketonów w roztworze kwaśnym. W chemii nieorganicznej lub analitycznej amalgamat cynku był i jest stosowany jako stosunkowo silny środek redukujący, m.in. B. do redukcji soli uranylu lub soli tytanylu, także do produkcji amalgamatów o mniejszej ilości metali nieszlachetnych z ich soli, np. B. amalgamatu miedzi, niklu lub kobaltu. W przeciwieństwie do czystego cynku lub innych stopów cynku, amalgamat cynku nie wytwarza wodoru; ponadto amalgamat cynku może być wolny od tlenków poprzez obróbkę kwasem. W przeszłości amalgamat cynku był również używany do mosiądzowania . W celu ochrony elektrod cynkowych w ogniwach galwanicznych przed korozją wraz z rozwojem wodoru, zostały one również połączone.
Inny
Amalgamat cyny tworzył odblaskową powłokę na lustrach aż do połowy XIX wieku .
Amalgamat może być stosowany jako substytut niezbędnej technicznie ciekłej rtęci w lampach energooszczędnych . Dzięki zastosowaniu amalgamatu strumień świetlny pozostaje prawie stały w większym zakresie temperatur. Ta zaleta jest szczególnie skuteczna w przypadku zastosowania w oprawach zamkniętych, obudowach kulistych i na zewnątrz. Wadą jest niski początkowy strumień świetlny zaraz po włączeniu, ponieważ rtęć odparowuje z amalgamatu tylko w wyższych temperaturach.
Lista pierwiastków tworzących amalgamat
Elementy są tutaj wymienione według (głównych i drugorzędnych) grup oraz liczebników porządkowych.
| H | Hej | |||||||||||||||||
| Li | Być | B. | DO. | N | O | FA. | Nie | |||||||||||
| nie dotyczy | Mg | Glin | Si | str. | Św. | Cl | Ar | |||||||||||
| K | Około | Sc | Ti | V | Cr | Mn | Fe | Współ | Ni | Cu | Zn | Ga | Ge | Tak jak | Se | Br | Kr | |
| Rb | Sr | Tak | Zr | Nb | pon | Tc | Ru | Rh | Pd | Ag | Płyta CD | W | Sn | Sb | Te | JA. | Xe | |
| Cs | Ba | La | * | Hf | Ta | W. | re | Os | Ir | Pt | Au | Ed | Tl | Pb | Bi | Po | W | Marg |
| Ks. | Ra | Ac | ** | Rf | Db | Sg | Biustonosz | Hs | Mt | Ds | Rg | Cn | ||||||
| * | Ce | Pr | Nd | Po południu | Sm | Eu | Bóg | Tb | Dy | Ho | On | Tm | Yb | Lu | ||||
| ** | Cz | Rocznie | U | Np | Puchatek | Na | Cm | Bk | cf | To | Fm | Md | Nie | Lr | ||||
Próbka amalgamatu
W przeciwieństwie do rtęci metalicznej i amalgamatu sole rtęci są wysoce toksyczne ze względu na ich rozpuszczalność w wodzie. Jest on wykrywany przez tak zwaną próbkę amalgamatu: Roztwór kwasu azotowego umieszcza się na miedzianej blasze – pozostaje srebrzysta plama amalgamatu, której nie można zetrzeć:
- Reakcja redoks : Kationy rtęci utleniają miedź do jonów miedzi i rtęci.
Rtęć tworzy stop z blachą miedzianą, amalgamat miedzi. Sole srebra tworzyłyby podobne plamy; jednak powstałe srebro można zetrzeć. Tak więc ostatecznie sole srebra można odróżnić od soli rtęci.
Proces amalgamatowy
W elektrolizie chloro-alkalicznej do produkcji chloru , sody kaustycznej i gazowego wodoru na dużą skalę , rtęć jest używana jako katoda w procesie amalgamatu , dzięki czemu sód powstały ze słonej wody w wyniku redukcji osadza się jako amalgamat. Amalgamat sodu przechodzi następnie do urządzenia do rozkładu amalgamatu, gdzie reaguje z wodą, tworząc wolny od soli wodorotlenek sodu, gazowy wodór i rtęć. Ten proces elektrolizy ma tę zaletę, że dostarcza wodorotlenek sodu (sodę kaustyczną) wolny od chlorku sodu, ale jest wątpliwy pod względem ekologicznym, ponieważ pozostałości rtęci muszą zostać usunięte z produktów (po oczyszczeniu, detoksykacji, np. za pomocą filtrów z węglem aktywnym).
Zobacz też
literatura
- Wolf-Dieter Müller-Jahncke : Amalgamat w alchemii. W: Werner E. Gerabek , Bernhard D. Haage, Gundolf Keil , Wolfgang Wegner (red.): Enzyklopädie Mediizingeschichte. De Gruyter, Berlin / Nowy Jork 2005, ISBN 3-11-015714-4 , s. 49.
- Curt Gerhard Lorber: Amalgamat w stomatologii. W: Werner E. Gerabek i in. (Red.): Encyklopedia Historia medyczna. 2005, s. 49 i n.
linki internetowe
Indywidualne dowody
- ↑ Jörg Barke: Język Chymiego: na przykładzie czterech rycin z lat 1574-1761. (= Językoznawstwo niemieckie. 111). Tybinga 1991, s. 357 n.
- ↑ Atlas mineralny: amalgamat
- ↑ Jak leczy się próchnicę? W: centrum doradztwa konsumenckiego . 23 stycznia 2018, dostęp 7 września 2020 .
- ↑ Niewiele dowodów na powiązanie wypełnień rtęciowych z problemami zdrowotnymi człowieka. (PDF; 25 kB). Komunikat prasowy LSRO dotyczący badania
- ↑ Wypełnienia zębów wykonane z amalgamatu są nieszkodliwe. W: Świat. 14 grudnia 2004 r.
- ↑ Lustra historyczne. pod adresem: spiegelart.de , dostęp 24 listopada 2015 r.
- ↑ ABC Chemie, Brockhaus-Verlag Lipsk, 1965, NRD, wpis „Amalgame” s. 60 i/lub pod odpowiednimi nazwami elementów
- ↑ Hollemann / Wiberg: Textbook of Inorganic Chemistry, wydanie 90, wpisy dotyczące właściwości poszczególnych pierwiastków